جامعة التعلم الافتراضي مؤسسة تعليمية غير ربحية عبر الإنترنت تأسست في بداية جائحة كوفيد-19، حيث انضم إليها طوعاً عدداً من الزملاء والأصدقاء من جامعات مغربية وأوروبية، وكذلك الولايات المتحدة وكندا وتركيا. المنصة تستهدف طلاب الدراسات العليا الهندسية وطلاب مرحلة الماجستير والدكتوراه. نركز على الفهم العميق للطاقة المتجددة وتخزين الطاقة; والهيدروجين الأخضر; وتغير المناخ والاحتباس الحراري; ومعالجة المياه وإعادة استخدامها; وتقنيات تحلية المياه وغيرها من المواضيع ذات الأهمية
نحن ممتنون جدًا لزملائنا، ونشكرهم جزيل الشكر على لطفهم وكرمهم في منح وقتهم ودعمهم لجامعة التعلم الافتراضي








أستاذ سالم رجب زايد عمر
الأستاذ سالم رجب زايد عمر، المدير التنفيذي لمركز سبائك للتعليم والتدريب (مملكة البحرين) برامج تعليمية وتدريبية واجتماعية
البروفيسور عبد الإله بن يوسف
أكاديمية الحسن الثاني للعلوم والتكنولوجيا، الرباط، المغرب أكاديمية الحسن الثاني للعلوم والتكنولوجيا، الرباط، المغرب كلية العلوم، جامعة محمد الخامس، الرباط، المغرب
بدر إيكن (الهندسة الميكانيكية)
الرئيس التنفيذي لشركة جي 3 / شريك إداري في شركة جي 2 / رئيس مجلس الأعمال المغربي الألماني - CGEM عضو مجلس إدارة غرفة التجارة الألمانية AHK المغرب
الدكتور إسماعيل أكالاي
المدير العام لمجموعة سوناسيد والمدير العام السابق لإدارة الكوبالت والمعادن الأساسية المدير العام السابق لإدارة الكوبالت والمعادن الأساسية


البروفيسور إسماعيل سعدون
أستاذ في جامعة محمد السادس متعددة التخصصات المغرب


البروفيسور صالح خمليش
مركز التميز البحثي مركز التميز البحثي في جامعة محمد السادس متعددة التقنيات المغرب


البروفيسور أحمد إهلال
جامعة ابن زهر، كلية العلوم،
خبير مقيّم في مجال الطاقات المتجددة لدى المركز الوطني للبحث العلمي والتقني
سيداتي وسادتي
أود أن أغتنم هذه الفرصة لأهنئ جميع زملائنا وأصدقائنا لمساهمتهم الفكرية في هذا المشروع النبيل.
كما تعلمون أن جائحة فيروس كورونا كوفيد -19 في العالم أثرت على كل جانب من جوانب مجتمعنا وشهد نظامنا التعليمي تغييرات ضخمة. .هكذا ولدت جامعة التعلم الافتراضي وتطورت لتحقيق ديمقراطية التعليم حيث ينقل التعليم إلى كل مواطن حيثما أراد وأينما شاء. وفقًا لخبرتنا واهتمامنا بالتدريس بما في ذلك البحث والتطوير نحن على استعداد لبناء هياكل وممارسات جديدة استمرت إلى ما بعد الوباء وأظهرت كيف تفيد هذه الجامعة الطلاب في المستقبل. لقد وضعنا تصورًا لجامعتنا وفقًا لاهتمامنا بالتكنولوجيا الخضراء والتنمية المستدامة، واستكشاف ما هو حاسم لتقوية البحث والتطوير من أجل إدخال تحسينات وابتكارات كبيرة في نظامنا التعليمي مع المعرفة والمهارات الجديدة بهدف الحصول على تدريب في مهارة ما وإعداد جيل جديد لوظائف جديدة، وتقنيات خضراء لحل المشكلات الناشئة والمتعلقة بالتنمية المستدامة والطاقة المتجددة والبيئة، والعلوم والتقنيات. فلسفتنا مبنية اساسا على مبدأ المرونة لتزويد المتعلمين بالمهارات اللازمة ويسمح لهم بتحديد ما يرغبون تعلمه، ولمذا وكيف ومتى ليصبحوا مواطنين فاعلين، مسؤولين ومشاركين ، فهذه مسؤولية مشتركة لاغتنام الفرص وإيجاد الحلول
العمل الذي تقومون به مهم للغاية


الأستاذ الدكتور أحمد الناوي - مؤسس جامعة التعلم الافتراضي
ندوات عبر الإنترنت من أرشيف جامعة التعلم الافتراضي
نبدأ هذه الصفحة الإلكترونية بندوات عبر الإنترنت للبروفيسور صبري قيس، الذي يتحدث عن التعلم الآلي الكمي للأنظمة المعقدة والحاسوب الكمي
حصل صبري قيس على درجة البكالوريوس والماجستير والدكتوراه من الجامعة العبرية في القدس في أعوام 1983 و1984 و1989 على التوالي. من 1989 إلى 1994، عمل باحثًا مشاركًا في جامعة هارفارد، قسم الكيمياء. ثم التحق بجامعة بردو بولاية إنديانا عام 1994 حتى عام 2024، حيث شغل منصب أستاذ متميز في الكيمياء والهندسة الكهربائية وهندسة الحاسوب والكهرباء، وأستاذ علوم الحاسوب والفيزياء. نشر أكثر من 290 بحثاً في مجلات علمية محكمة. يكرس أبحاث مجموعته بشكل رئيسي للمعلومات الكمية والحوسبة الكمية للأنظمة المعقدة. وهو زميل الجمعية الفيزيائية الأمريكية، وزميل الجمعية الأمريكية لتقدم العلوم، وزميل الجمعية الأمريكية لتقدم العلوم، وزميل غوغنهايم، وباحث في هيئة التدريس بجامعة بردو، وزميل في جائزة مؤسسة العلوم الوطنية، وجائزة سيجما شي للأبحاث لعام 2012، وجائزة هربرت نيوباي ماكوي لعام 2019، جامعة بردو


الأستاذ الدكتور صبري قيس
كرسي جودنايت المتميز في الحوسبة الكمية، قسم الهندسة الكهربائية وهندسة الحاسبات، جامعة ولاية كارولينا الشمالية


أما الندوة الثانية فيقدمها البروفيسور إيفان جوردون بعنوان تكنولوجيا الخلايا والوحدات الكهروضوئية السيليكونية المستدامة في عصر التيراوات
حصل إيفان جوردون على درجة الدكتوراه في مجال المواد المغناطيسية الجديدة لتطبيقات أجهزة الاستشعار من جامعة لوفين، بلجيكا في فبراير 2002. بدأ العمل في مجال الخلايا الكهروضوئية في يونيو 2003 في المركز الدولي للتكنولوجيا المتكاملة. ويقود حالياً مجموعة التكنولوجيا الكهروضوئية وأنظمة الطاقة في معهد IMO-IMOMEC. بالإضافة إلى ذلك، يعمل أيضاً أستاذاً غير متفرغ للخلايا الكهروضوئية الرقمية في جامعة دلفت للتكنولوجيا في هولندا ورئيس تحرير المجلة العلمية الدولية لمواد الطاقة الشمسية والخلايا الشمسية. منذ يناير 2016، وهو منسق البرنامج المشترك حول الخلايا الكهروضوئية التابع للتحالف الأوروبي لأبحاث الطاقة (EERA) وعضو اللجنة التوجيهية للمنصة الأوروبية للتكنولوجيا والابتكار في مجال الخلايا الكهروضوئية. قام بتأليف والمشاركة في تأليف أكثر من 240 بحثاً في المجلات والمؤتمرات (حوالي 4500 استشهاد، عامل ح 36، أكتوبر 2024). وهو عضو في اللجنة العلمية للعديد من المؤتمرات الدولية (مثل المؤتمر الأوروبي للطاقة الشمسية الكهروضوئية الأوروبية، ومؤتمر أخصائيي الطاقة الشمسية الضوئية التابع لمعهد مهندسي الكهرباء والإلكترونيات IEEE، ومؤتمر السيليكون الكهروضوئية، والمؤتمر الدولي للطاقة المتجددة والمستدامة، ) وقدم بنفسه أكثر من 30 محاضرة مدعوة في المؤتمرات وورش العمل والمدارس الدولية.


الأستاذ الدكتور إيفان جوردون
أستاذ الخلايا الكهروضوئية الرقمية في جامعة دلفت التقنية


المؤتمر الثالث عبر الإنترنت للأستاذ الدكتور محمد نظير الدين، أستاذ ومدير مختبر الهندسة الجزئية في جامعة البوليتكنيك الفيدرالية في لوزان، سويسرا حول هندسة التخليق الهندسي لخلايا البيروفسكايت الشمسية الفعالة والمستقرة
محمد خاجة نظير الدين أستاذ الكيمياء في المعهد التقني الفدرالي العالي في لوزان في سيون، وتركز أبحاثه الحالية في المعهد على الخلايا الشمسية البيروفسكايتية والصمامات الثنائية الباعثة للضوء. وقد نشر أكثر من 785 ورقة بحثية تمت مراجعتها من قِبل الأقران، وعشرة فصول في كتب، وهو مخترع/مشارك في أكثر من 90 براءة اختراع. وقد تم الاعتراف بالتأثير الكبير لعمله من خلال دعوات للتحدث في أكثر من 300 مؤتمر دولي. ظهر اسمه في قائمة ISI للكيميائيين الأكثر استشهاداً ولديه مؤشر هيرش 196. يقوم محمد نظير الدين بتدريس مقرر ”المواد الوظيفية“ في المعهد التقني الفدرالي العالي بلوزان وجامعة كوريا. ووفقًا لموقع منصة Web of Science، فهو خامس أكثر الكيميائيين استشهادًا في العالم وهو واحد من بين 19 عالمًا حددتهم تومسون رويترز كأكثر العقول العلمية تأثيرًا في العالم في عام 2015، كما تم إدراجه ضمن أفضل 10 باحثين في مجال أبحاث الخلايا الشمسية البيروفسكايت من قبل مؤسسة تايمز للتعليم العالي. يقوم بتوجيه وإدارة العديد من المشاريع الصناعية والوطنية ومشاريع الاتحاد الأوروبي. تم تعيينه أستاذًا جامعيًا عالميًا من قبل جامعة كوريا وأستاذًا مساعدًا من قبل جامعة الملك عبد العزيز بجدة. انتُخب عضواً في الأكاديمية الأوروبية للعلوم، وزميلاً للجمعية الملكية للكيمياء، وزميلاً لأكاديمية تيلانجانا للعلوم، كما فاز بجائزة الخوارزمي الدولية الرابعة والثلاثين في العلوم الأساسية لعام 2021.


الأستاذ الدكتور محمد خاجة نظير الدين
المعهد الفدرالي السويسري للتكنولوجيا، لوزان


كل شيء عن البيروفسكيت
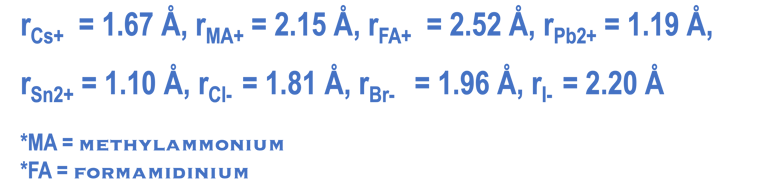
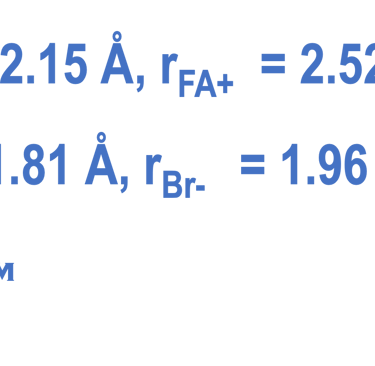
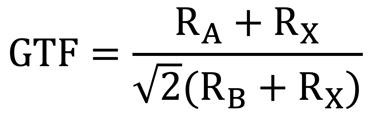
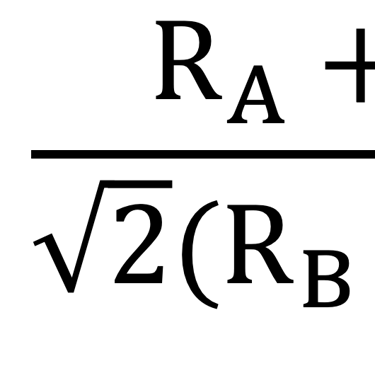
Goldschmidt Tolerance Factor (GTF) rule
قاعدة عامل التسامح لجولدشميت
البيروفسكايت هو فئة من المواد لها بنية بلورية مشابهة لمعدن البيروفسكايت، أكسيد الكالسيوم تيتانيوم (CaTiO₃)
الصيغة العامة للبيروفسكايت هي ABX₃، حيث ”A“ و”B“ كاتيونات مختلفة الأحجام، و”X“ أنيون مرتبط بكليهما
تُعرف مواد البيروفسكايت بخصائصها الكهربائية والإلكترونية المواتية جدًا في تطبيقات متنوعة، خاصة في الخلايا الكهروضوئية
يتكون هيكل البيروفسكايت من خلية وحدة مكعبة، حيث الكاتيو "A" في زوايا المكعب، والكاتيون "B" في وسط الخلية، والأنيونات "X" عند الحواف (نقاط المنتصف)
تملأ الكاتيونات الكبيرة، مثل MA وFA العضويين، الفراغات الثماني الأوجه وتعوض الشحنة السالبة، وتوازن الشحنة الكلية لضمان استقرار الشبكة
أثبت تجريبياً، لتحقيق الاستقرار الهيكلي في نظام بيروفسكايت ثلاثي الأبعاد ”عامل تحمل غولدشميدت GTF“ التالي فيما يتعلق بأنصاف أقطار الكاتيون والأنيون
هناك مجموعة واسعة من الكاتيونات والأنيونات يمكن أن تعطي مجموعة واسعة من مواد البيروفسكايت وفقًا لهذه القاعدة
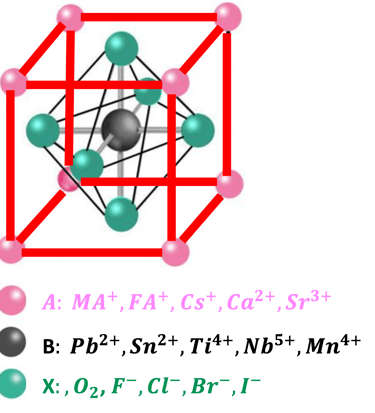
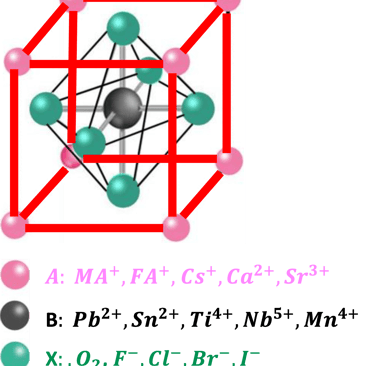
Reference:
Chun-Ho Lin et al. Advanced Materials 2022, 34, 2108616 // O. Grånäs, D. Vinichenko, & E. Kaxiras, Establishing the limits of efficiency of perovskite solar cells from first principlesmodeling. Sci Rep 6, 36108 (2016) // https://www.science.org/doi/10.1126/sciadv.aav0693 // https://encyclopedia.pub/entry/42834
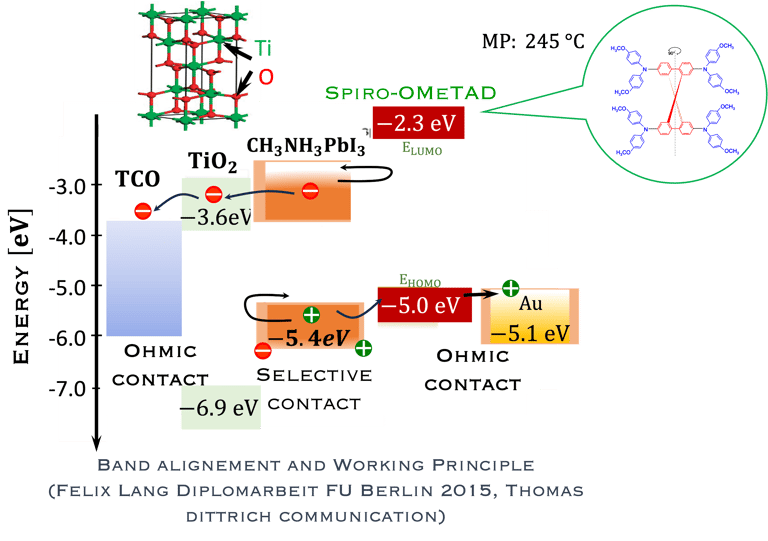
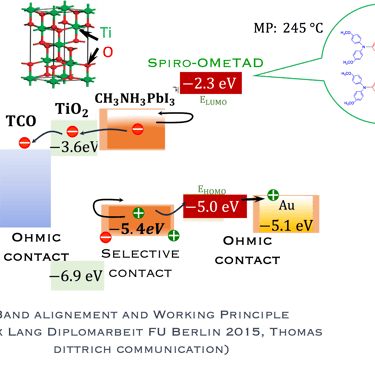
أهم إيجابيات البيروفسكايت إضافةً لانخفاض سعرها مقارنةً بالسيليكون
سهلة التصنيع وتجميع الطبقات في عمليات منخفضة التكلفة
البيروفسكايت هو الطبقة الأكثر أهمية التي تمتص الضوء المرئي وتنتج الإلكترونات والثقوب التي يمكن تجميعها لإنتاج الكهرباء
ومع ذلك، من أجل تجميع الشحنات يجب اختيار الطبقات المناسبة من المواد المختلفة لتصنيع الخلايا الشمسية
يتطلب التجميع الفعال للإلكترونات والثقوب مواد نقل الشحنة
على سبيل المثال: مادة شفافة للضوء المرئي ولها موصلية للتيار الكهربائي تعرف باسم (TCO)
الطبقات الأخرى المعروفة باسم موصلات الإلكترونات والثقوب ETL وHTL
لا يزال البحث والتطوير جارياً لاستكشاف مواد جديدة فعالة لنقل الشحنات (للإلكترونات والثقوب) ذات خصائص محددة مثل المواد الصديقة للبيئة، والتصنيع الفعال من حيث التكلفة، ونقل الشحنات بكفاءة، والأهم من ذلك الاستقرار على المدى الطويل
يتطلب الفهم العميق لكيفية عمل خلايا البيروفسكايت الشمسية معرفة مخطط نطاق الطاقة لجميع المواد والمركبات التي تشكل الخلية الشمسية
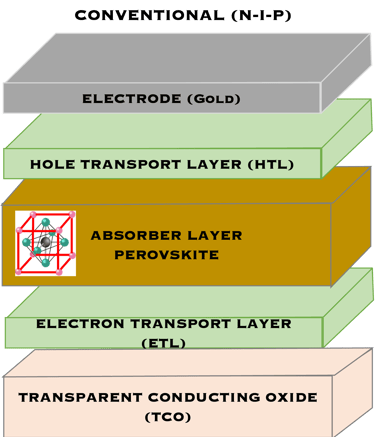
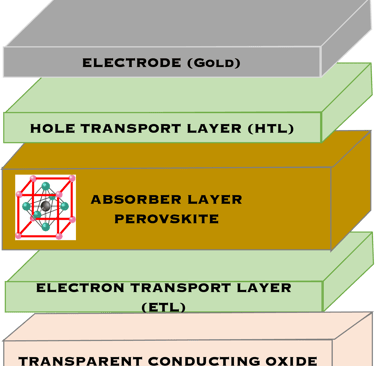
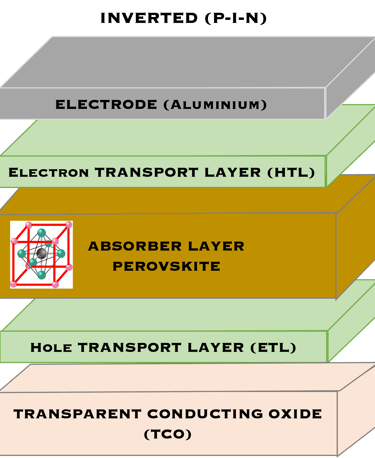
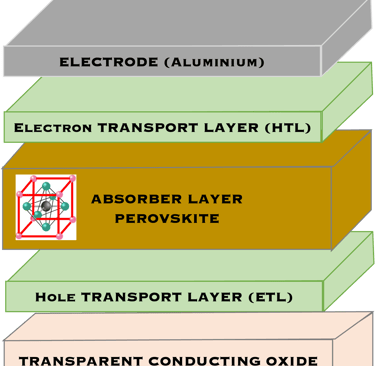
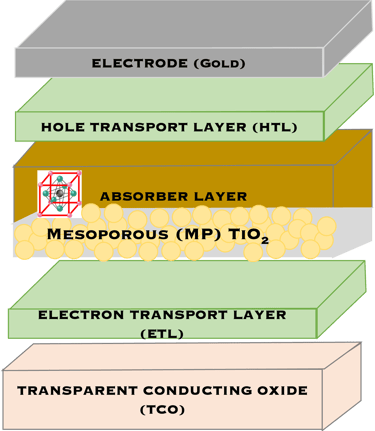
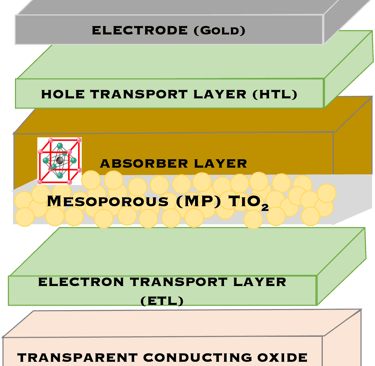
ثلاثة مخططات هيكلية نموذجية لخلايا البيروفسكايت الشمسية والتي يتم استكشافها بشكل مكثف من قبل العديد من الباحثين
مخطط مستوى الطاقة للبيروفسكايت بما في ذلك مواد الأقطاب الكهربائية لنقل الشحنة
يُستخدم سبيرو-أوميتاد عادةً كجهاز HTM في إنتاج خلايا البيروفسكايت الشمسية عالية الأداء.
يركز معظم البحث والتطوير على تصنيع خلايا شمسية ترادفية من السيليكون/البيروفسكايت، حيث يكون السيليكون هو الخلية الفرعية السفلية (فجوة النطاق 1.12 إلكترون فولت) والهدف هو زيادة الكفاءة إلى أقصى حد
لتحقيق ذلك، يجب أن تتراوح فجوة النطاق المثالية للخلايا العلوية بين 1.67 و1.75 إلكترون فولت
أظهرت البيروفسكايت أفضل خلية علوية حيث يمكن ضبط هذه المادة لتحقيق فجوة نطاق مختلفة
يمكن تصنيع البيروفسكايت باستخدام طرق كيميائية مثل الطلاء بالدوران، وتقنية الطباعة، وجميع هذه الطرق منخفضة التكلفة ولا تتطلب درجة حرارة عالية
تبلغ قيمة سمك البيروفسكايت حوالي 300-500 نانومتر كافية للخلية الفرعية للبيروفسكايت، في المقابل تتطلب طبقة السيليكون سمكًا أكبر بآلاف المرات بسبب فجوة النطاق غير المباشرة ومعامل الامتصاص المنخفض


الهدف من ترادف السيليكون/البيروفسكايت هو جمع أكبر قدر ممكن من الطيف الشمسي، وخاصة الأشعة المرئية والأشعة تحت الحمراء
في الوقت الحالي، تحقق العديد من المجموعات كفاءات أعلى من 30%
ترجمة هذه النتائج من المختبر إلى التصنيع هو الأكثر تحديًا في مجال البحث والتطوير
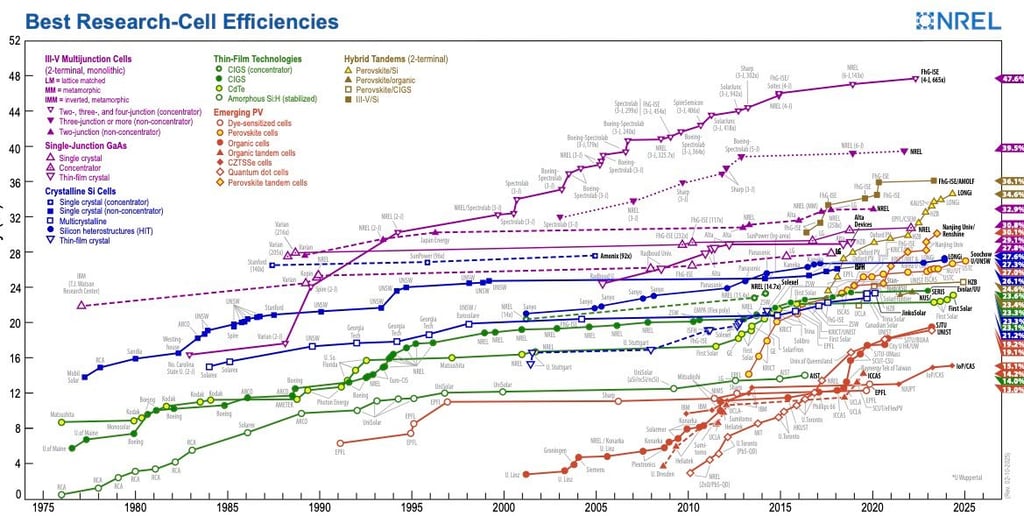
الخلية الشمسية الترادفية الأكثر كفاءة حتى الآن هي خلية ذات كفاءة 34.6% قدمتها الشركة الصينية لونجي في يونيو 2024 (source: https://www.fluxim.com/perovskite-silicon-tandem-pv-record-updates)
Record Solar cell efficiency from the 1980s to 2024, including the performance of Perovskite/Silicon tandem cells (NREL DATA) https://www.nrel.gov/pv/cell-efficiency.html
Green hydrogen production, through the splitting of water by Renewable electricity
إنتاج الهيدروجين الأخضر، من خلال تقسيم الماء بواسطة الكهرباء المتجددة


Prof. Thomas Hannappel
البروفيسور توماس هانابيل
Head of the department “Fundamentals of Energy Materials”
Dean of the Master course “Renewable Energy Techniques” at the Institute of Physics, Technische Universität (TU) Ilmenau
توماس هانابيل هو أستاذ فول، ورئيس قسم ”أساسيات مواد الطاقة“، وعميد دورة الماجستير ”تقنيات الطاقة المتجددة“ في معهد الفيزياء بجامعة إلميناو التقنية. حصل على درجة الدكتوراه من خلال دراسات حول ديناميكيات حاملات الشحنة المستحثة ضوئيًا التي أجراها في قسم ”الكيمياء الفيزيائية“ للبروفيسور غيرهارد إرتل في معهد فريتز هابر في برلين. أنشأ توماس نظامًا جديدًا ومبتكرًا لتحليل نمو أشباه الموصلات للحصول على مواد إلكترونية ضوئية عالية الأداء وتفاعلات بينية فيزيائية كيميائية معقدة لتطوير هياكل أجهزة عالية الكفاءة تحقق قيمًا قياسية عالمية لكفاءة تحويل الخلايا الشمسية وكذلك إنتاج الوقود الشمسي الأخضر.


يقدم هذه الندوة عبر الإنترنت حول الهيدروجين الأخضر والوقود الشمسي بالتمثيل الضوئي الاصطناعي البروفيسور توماس هانابيل، أحد الخبراء في هذا المجال
تحويل الطاقة الشمسية: التعلم من الطبيعة
هنا نلقي نظرة بالتفصيل الأكاديمي على هذا التحويل للطاقة الشمسية إلى كهرباء. كما شرح البروفيسور توماس هانابل بالتفصيل في ندواته السابقة, تُعرف الطريقة المباشرة لتحويل الطاقة الشمسية ب"التمثيل الضوئي الاصطناعي". ولا تزال عملية التمثيل الضوئي الاصطناعي في مرحلة البحث والتطوير، ولكن كما لاحظتم في الندوات، فإن التقدم واعد والمثال الذي طوره البروفيسور توماس باستخدام مركبات III-V من الجدول الدوري أظهرت بالفعل كفاءة تحويل الطاقة إلى هيدروجين بنسبة 19% على المستوى المختبري.
بالإضافة إلى التحويل المباشر للطاقة، سنسلط الضوء أيضًا على الطرق غير المباشرة لإنتاج الهيدروجين الأخضر، وهذا يتطلب ما نسميه ”تطوير المُحلِّلات الكهربائية“ وهو نظام يستخدم لتفكيك الماء إلى هيدروجين وأكسجين. وهذا يمكّن من إنتاج غاز الهيدروجين، وإطلاق الأكسجين المتبقي في الغلاف الجوي أو التقاطه أو تخزينه لتزويد العمليات الصناعية أو لإمداد المستشفيات بالأكسجين النظيف.
عملية تكرير النفط أو"المعالجة الهيدروجينية" لإزالة الكبريت وكسر سلاسل الكربون الطويلة إلى منتجات خفيفة وزيادة نسبة الهيدروجين إلى الكربون تنتج انبعاثات غازية ضارة بصحة الإنسان والبيئة وتحتاج إلى مراجعة لإيجاد حلول لتجميع وربما إعادة استخدام هذه الغازات السامة. وهناك حاجة إلى البحث والتطوير والابتكاري للحصول على اقتصاد مستدام
”الطاقة إلى X“ من أجل مستقبل مستدام وخالٍ من الكربون
تُستخدم التسمية ”هيدروجين أزرق“ في كل مرة يتم فيها التقاط ثاني أكسيد الكربون المنبعث ثم حقنه في مرافق تخزين على سبيل المثال طبقات المياه الجوفية المالحة أو خزانات النفط والغاز المستنفدة
عندما يتم استخراج الهيدروجين من الفحم أو الغاز الطبيعي باستخدام عملية تحويل الميثان بالبخار، نطلق عليه الهيدروجين الرمادي
”الهيدروجين الأخضر“ هو البديل للوقود الأحفوري، لاستخدامه بشكل مكثف في الصناعات كثيفة الاستهلاك للطاقة مثل: الصناعات الكيميائية أو الأسمنت أو الحديد والصلب. ويمثل حالياً 4% من الإنتاج العالمي
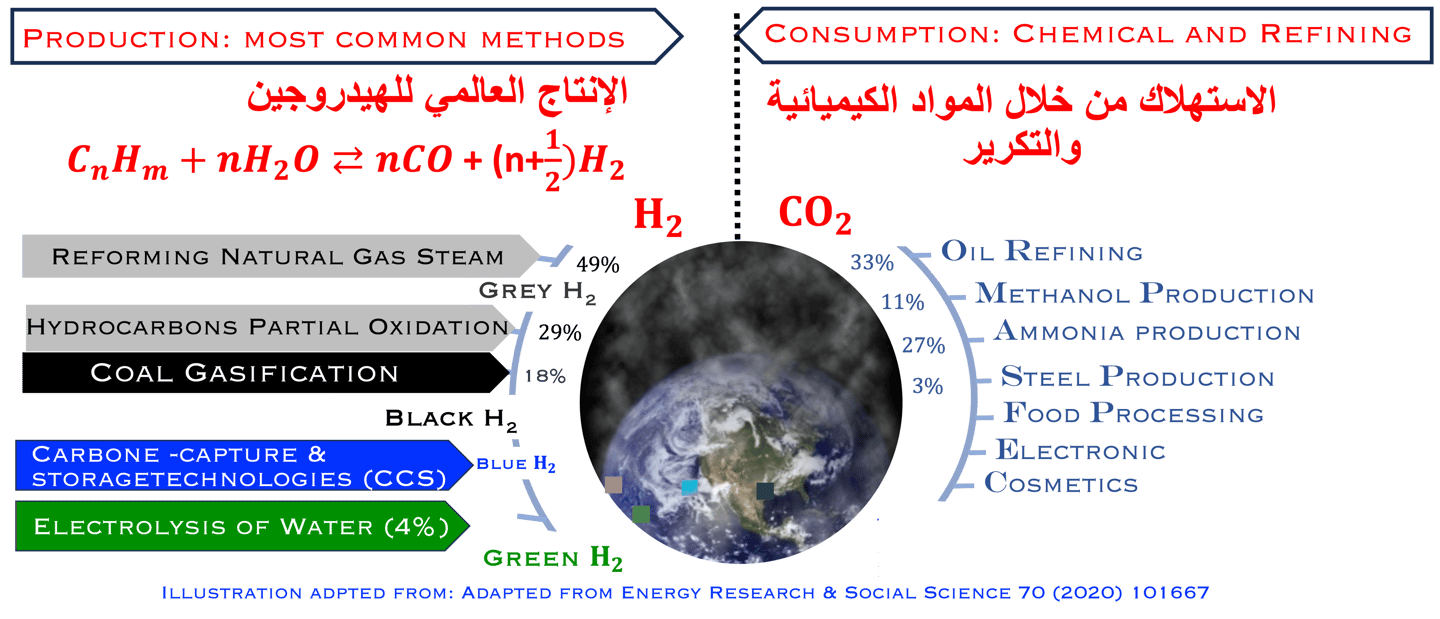
لا تزال صناعة إنتاج الهيدروجين من الغاز الطبيعي تهيمن على السوق مع حوالي الربع يأتي من الفحم والباقي من الغاز الطبيعي مما يُسبب تلوثًا بيئيًا كبيرًا ونتيجة لذلك، فإن الهيدروجين المنتج من الغاز الطبيعي في العالم ينبعث منه 830 مليون طن/سنة من ثاني أكسيد الكربون. وبلغ الطلب العالمي على الهيدروجين 97 مليون طن في عام 2023. يُستخدم الهيدروجين في قطاعي التكرير والكيماويات، وفي توليد الحرارة والطاقة. (بيانات الوكالة الدولية للطاقة المتجددة ووكالة الطاقة الذرية الأمريكية). من المهم أن نلاحظ أن إنتاج الهيدروجين المنخفض الانبعاثات بلغ أقل من مليون طن في عام 2023 ومن المتوقع أن يتزايد عدد المشاريع التي اتخذت قرار الاستثمار في إنتاج الهيدروجين من الطاقة المتجددة (الهيدروجين الأخضر والهيدروجين منخفض الانبعاثات)، حيث بلغت سعة التحليل الكهربائي المُعلنة حوالي 520 جيجاوات. كما يتزايد عدد المشاريع التي اتخذت قرار الاستثمار النهائي: فقد تضاعف الإنتاج المعلن عنه مقارنة بالعام الماضي ليصل إلى 3.4 مليون طن سنويًا، ويتوزع هذا الإنتاج بالتساوي تقريبًا بين التحليل الكهربائي (1.9 مليون طن سنويًا) والوقود الأحفوري مع التقاط الكربون واستخدامه وتخزينه (CCUS) (1.5 مليون طن سنويًا).
يوضح الرسم التوضيحي أدناه، المقتبس من المرجع*، الوضع الحالي لما يسمى بالطاقة إلى ”X“ من حيث إنتاج الهيدروجين واستهلاكه
*Energy Research & Social Science 70 (2020) 101667
تُستخدم التكنولوجيا الكهروضوئية لإنتاج الكهرباء، ويمكن حقن فائض الكهرباء الذي لا يتم استخدامه في المحلل الكهربائي لإنتاج الهيدروجين الأخضر الذي يتم تخزينه واستخدامه في حالة عدم وجود أو انخفاض أشعة الشمس
التحليل الكهربائي للمياه باستخدام الكهرباء المولدة من الطاقات المتجددة لإنتاج الهيدروجين الأخضر هي أفضل تقنية لإنتاج الوقود بدون انبعاث غازات كربونية
لتفادي النقل لمسافات طويلة، يمكن إنتاج الهيدروجين الأخضر بالقرب من الصناعات كثيفة الاستهلاك للطاقة مثل الصناعات الكيميائية أو الأسمنت أو الحديد والصلب ويمكن تطبيقه وهو أفضل بديل للوقود الأحفوري.
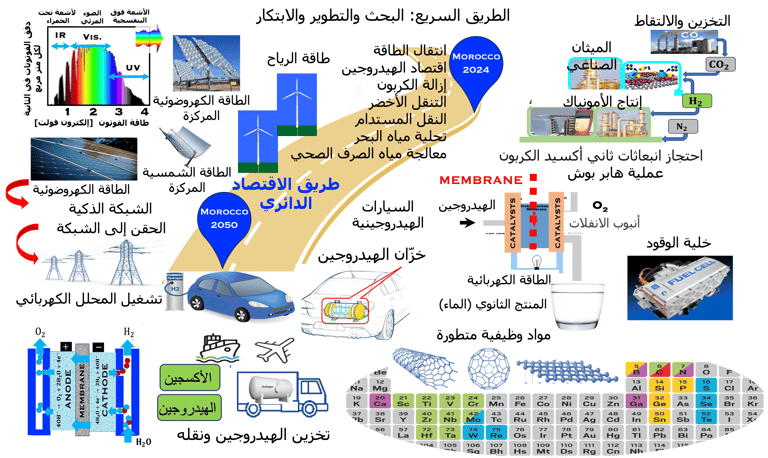
وأهم استخدام للهيدروجين الأخضر هو ما يسمى بعملية هابر-بوش، حيث يتم تحويل النيتروجين الجوي إلى أمونيا، وفي الوقت الحالي، يتم إنتاج معظم الأمونيا باستخدام الهيدروجين الذي يتم توفيره من تفاعل تكسير الغاز الطبيعي (الميثان)، والذي ينتج كميات كبيرة من ثاني أكسيد الكربون
ويشمل الرسم أدناه، عناصر مختلفة تحتاج إلى برنامج تطوير البحوث الأساسية والمعرفة بما في ذلك نقل وترقية العملية الصناعية
من المحاور المهمة في مجال البحث والتطوير، استكشاف محفزات كهربائية جديدة من خلال المحاكاة والنمذجة قبل إجراء التجارب المكثفة التكلفة
خلايا الوقود ومواد تخزين الهيدروجين من الموضوعات التي يجب إدراجها في المناهج البحثية والجامعية ة
أغشية التبادل البروتوني لإنتاج الهيدروجين عن طريق المحلل الكهربائي القلوي وغشاء التبادل البروتوني (PEM) بحاجة إلى البحث والتطوير لخفض التكلفة وزيادة الكفاءة
من خلال هذا التوضيح، نود أن نؤكد على أن خريطة الطريق لتحقيق هدف الانبعاثات الصفرية الصافية بحلول عام 2050 تتطلب نهجًا متعدد التخصصات يشمل الإرادة السياسية ومفهومًا جديدًا للتعليم والبحث والتطوير
المقدمة: التحويل الكهروكيميائي للطاقة الشمسية: التعلم من الطبيعة
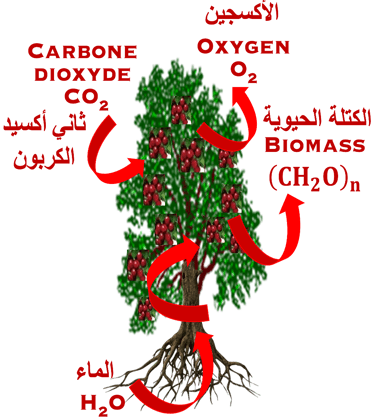
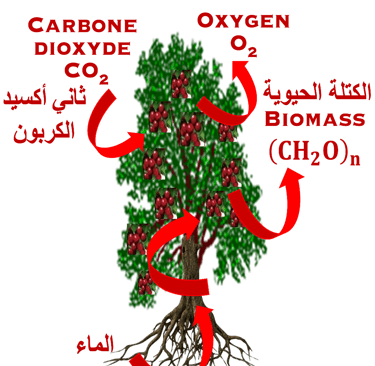
البناء الضوئي، هي العملية التي تقوم بها النباتات بالتقاط الطاقة الشمسية من خلال الكلوروفيل وتحويل ثاني أكسيد الكربون مع الماء إلى كربوهيدرات ومركبات أخرى
الماء الذي تنقله الجذور، وثاني أكسيد الكربون الذي يمر عبر ثغور الأوراق، وأشعة الشمس هي العناصر الأساسية لعملية التمثيل الضوئي


هناك أيضًا تنفس هوائي يحدث في الميتوكوندريا ويتطلب الأكسجين والجلوكوز، وينتج ثاني أكسيد الكربون والماء والطاقة في شكل كتلة حيوية.


باختصار، ضوء الشمس والماء والكلوروفيل والإنزيمات المساعدة هي في قلب دورة التمثيل الضوئي التي تنتج الكتلة الحيوية (مثل الجلوكوز) وتطلق الأكسجين في الغلاف الجوي. السؤال: هل يمكننا إنتاج عملية البناء الضوئي في المختبر؟ الإجابة هي نعم
البناء الضوئي الاصطناعي هي تقنية مستدامة تحاكي الطريقة التي تحول بها النباتات ضوء الشمس إلى طاقة كيميائية قابلة للتخزين. الهدف هو التوصل إلى طريقة أفضل وأوسع نطاقاً لإنتاج الطاقة النظيفة وتجنب الوقود الأحفوري مثل النفط والغاز والفحم وهذا سيساعد بشكل كبير في التخفيف انبعاثات غازات الاحتباس الحراري
فيما يلي نسلط الضوء على عملية تحلل الماء وإنتاج الهيدروجين الأخضر بواسطة العملية الكهروضوئية باستخدام أشباه الموصلات والإلكتروليتات المائية
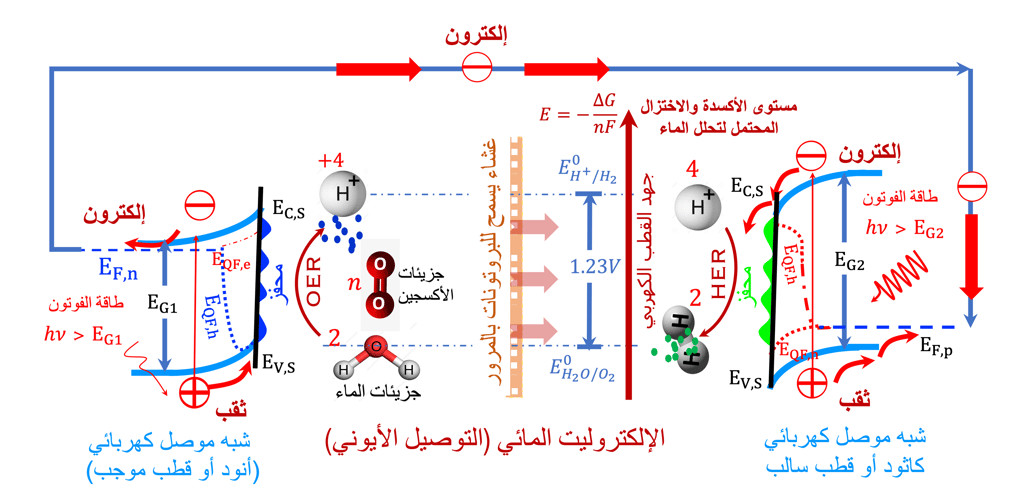
تتميز أشباه الموصلات بنطاق التكافؤ المملوءة بالإلكترونات ونطاق التوصيل الفارغة من الالكترونات
يتم امتصاص ضوء الشمس بواسطة الإلكترونات الموجودة في نطاق التكافؤ وعندما تكون طاقة الفوتونات أكبر من فجوة النطاق أو تساويها على الأقل، فإن الإلكترونات تقفز إلى نطاق التوصيل
تم استخدام نوعين من أشباه الموصلات في الرسم التوضيحي:
النوع (N) الذي يعمل كقطب موجب (أنود)
النوع (P) الذي يعمل كقطب سلبي (كاثود)
يختلف النوع (N) عن النوع (P) في التوصيل الكهربائي. يرجى الرجوع إلى كتب أشباه الموصلات أدناه (أو ندواتي عبر الإنترنت السابقة) لمعرفة المزيد عن مفهوم الموصلات (N) و (P)
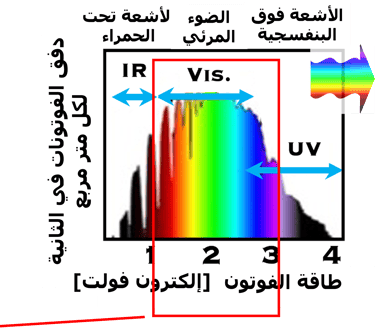
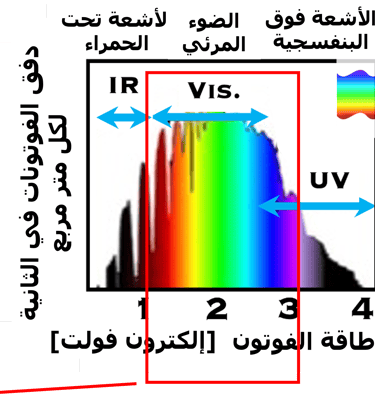
من الواضح أن امتصاص المزيد من الفوتونات عند الأقطاب يؤدي إلى زيادة عدد الإلكترونات لإنتاج الهيدروجين
لجمع جزء كبير من الطيف الشمسي، نحتاج إلى استخدام العديد من أشباه الموصلات (ارجع إلى ندوة المؤتمر عبر الإنترنت لتوماس هانابيل حول الأقطاب الكهربائية متعددة الوصلات)


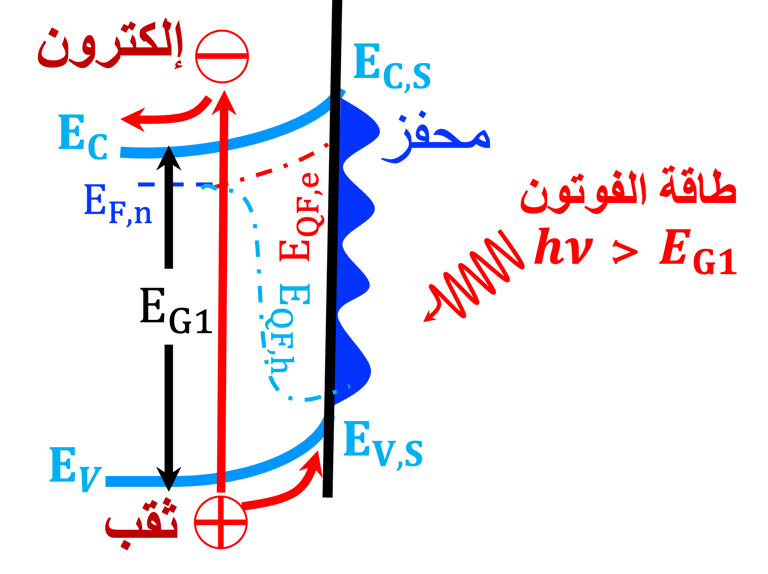
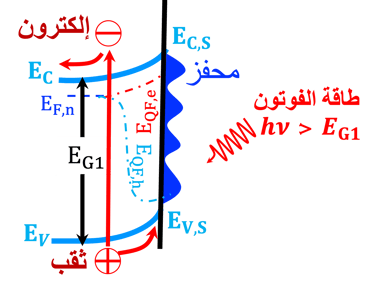
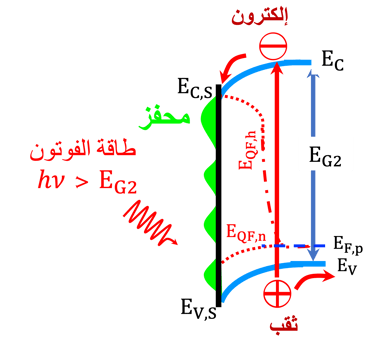
يوضح الرسم البياني (على اليسار) أشباه الموصلات من النوع (N) تحت الإضاءة باستخدام فوتونات لها طاقة تساوي أو أكبر من فجوة النطاق.
تتضمن عملية امتصاص الفوتون انتقال الإلكترونات إلى نطاق التوصيلنتيجة لذلك، يتم إنشاء فجوات (أو غياب للإلكترونات) في نطاق التكافؤ
تحدد طبيعة الشحنة الكهربائية السائدة في منطقة واجهة أشباه الموصلات/الإلكتروليت اتجاه حركة الشحنات الكهربائية (توضح الأسهم اتجاهات الإلكترونات والثقوب)
اتجاه حركة الثقوب
اتجاه حركة الإلكترونات
بالنسبة لأشباه الموصلات من النوع (N)، تتجه الإلكترونات إلى الداخل وتتجه الثقوب إلى السطح
تتمتع الثقوب بقوة أكسدة ويمكنها أكسدة الكيانات الموجودة على سطح الأنود (القطب الموجب)
تتدفق الإلكترونات نحو الكاثود (القطب السالب) عبر الدائرة الخارجية،





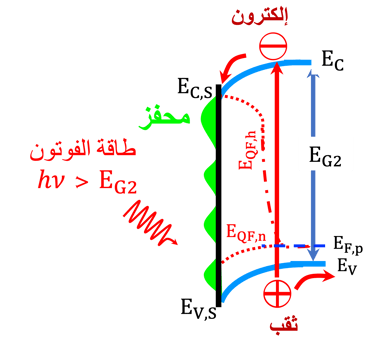
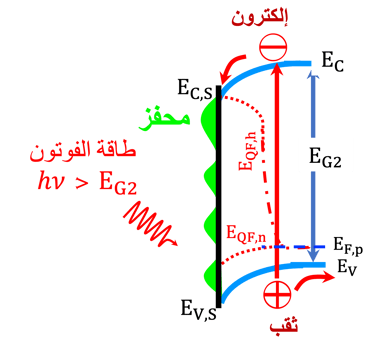
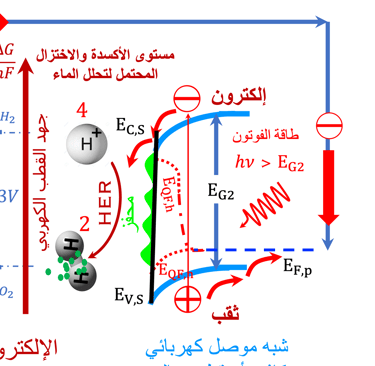
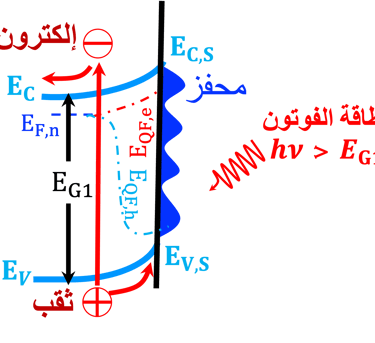
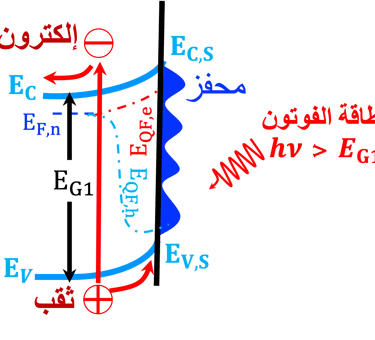
يوضح الرسم البياني (على اليمين) أشباه الموصلات من النوع (P)، تحت الإضاءة باستخدام فوتونات لها طاقة تساوي أو أكبر من فجوة النطاق لمادة أشباه الموصلات من النوع (P)
على غرار أشباه الموصلات (N)، تتضمن عملية امتصاص الفوتون في القطب السالب (نوع P) انتقال الإلكترونات من نطاق التكافؤ إلى نطاق التوصيل
اتجاه حركة الالكترونات نحو السطح
اتجاه حركة الثقوب إلى داخل القطب
تتفاعل الإلكترونات الموجودة على سطح القطب السالب (الكاثود) مع البروتونات الموجودة في الماء، ونتيجة لذلك يتشكل الهيدروجين















من المهم أن نذكر العناصر الأساسية لتحويل الطاقة الشمسية المباشرة من خلال انقسام الماء إلى أكسجين وهيدروجين باستخدام العملية الكهروكيميائية
1) الأقطاب الكهربائية لأشباه الموصلات ذات فجوات النطاق الملائمة
2) العوامل الحفازة التي تسهل التفاعلات الكهروكيميائية
3) الأغشية الانتقائية التي تسمح بمرور البروتونات من خلالها
الأغشية الانتقائية
مصدر الجهد الكهروضوئي في الخلية الكهروضوئية الكيميائية
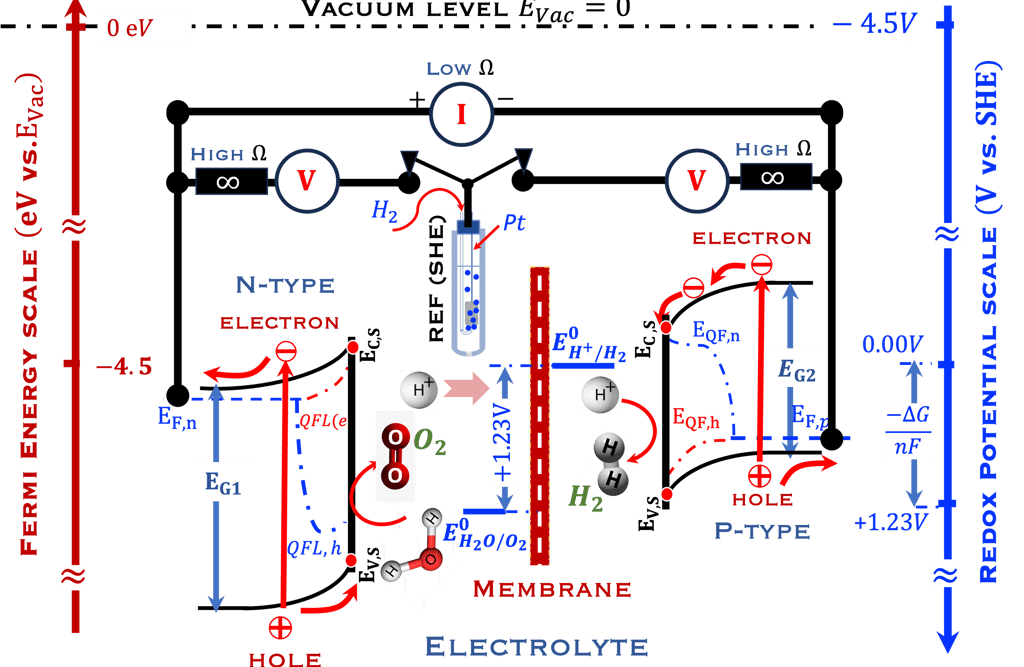
لفهم أصل الجهد الضوئي بعمق، يجب أن ننظر إلى الفيزياء الإحصائية لأشباه الموصلات، مع الأخذ في الاعتبار نوعي (N و P)، كما هو موضح في الرسم التخطيطي. في حقيقة الأمر في حالة الاتزان الحراري (Thermal Equilibrium) يخضع عدد الإلكترونات (n) والثقوب (p) في أشباه الموصلات لإحصائية فيرمي-ديراك (الإلكترونات فرميونات)
نعرض أدناه (على اليمين) مخطط الطاقة لأنود شبه موصِّل (من النوع N) بدون إضاءة في حالة اتزان ديناميكي حراري مع نظام أكسدة واختزال و نعرض كذلك التغيرات التي تطرأ على عدد الإلكترونات (n) والثقوب بدون إضاءة والموجودة في مستوي طاقة معيَّنة والمعادلات الرياضيات التي تتغير تحت الإضاءة إلى (*n) و (*p). يمكننا بعد ذلك استنتاج طاقة شبه فيرمي للإلكترونات والفجوات:
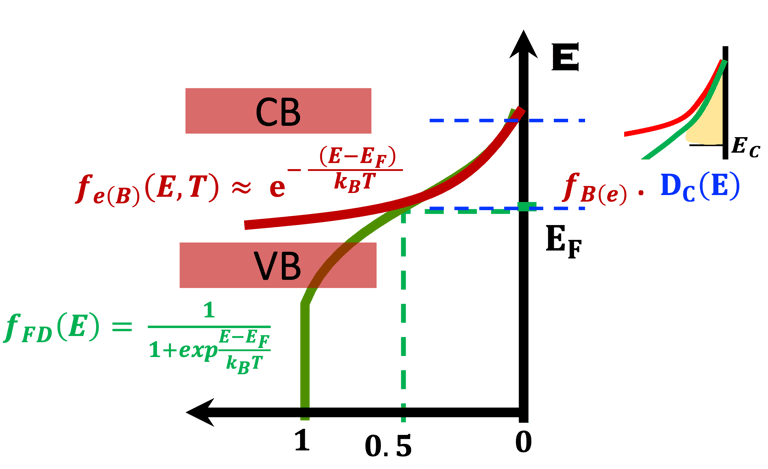
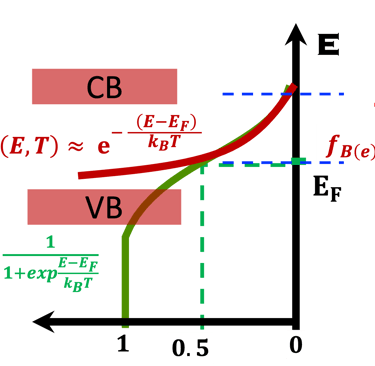
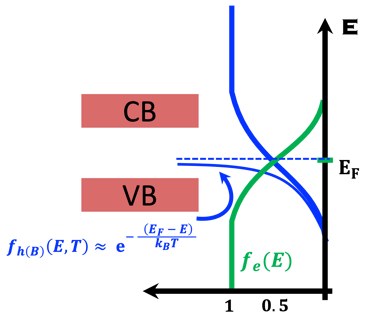
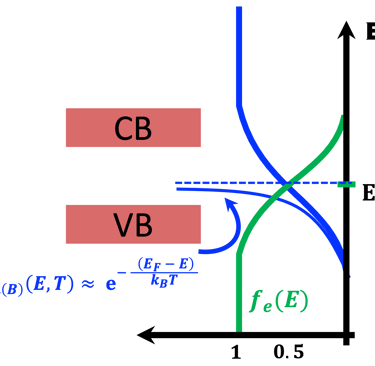
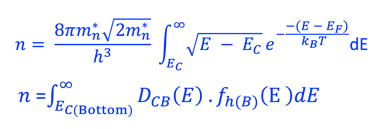
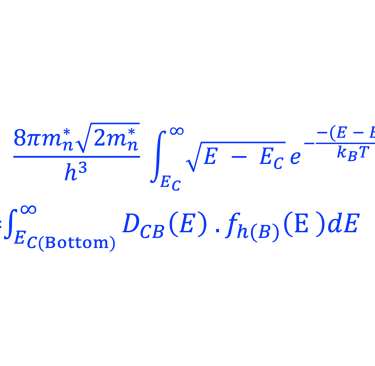
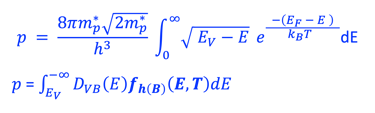
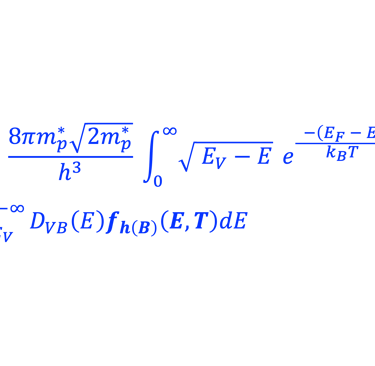
غالبًا ما تُستخدم إحصائيات ماكسويل-بولتزمان كتقريب للحقيقة (التفاصيل في الرسم التوضيحي أدناه)
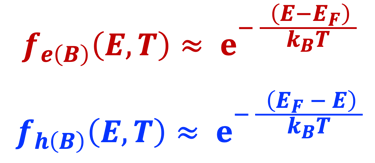
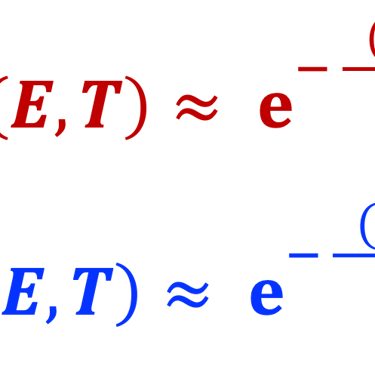
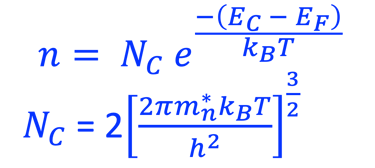
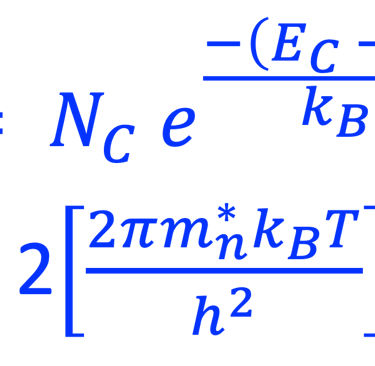
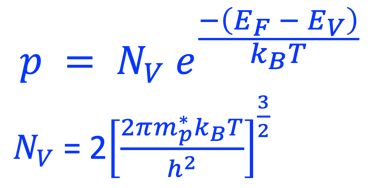
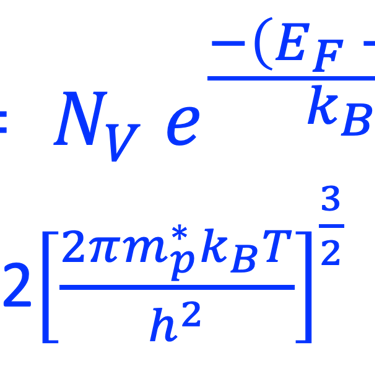
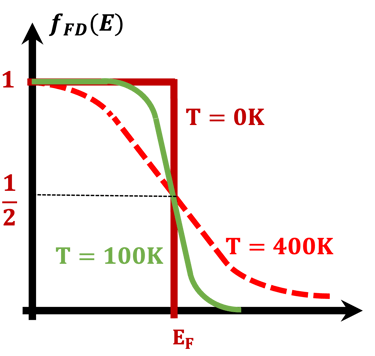
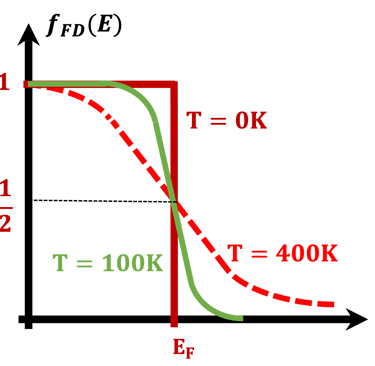
يوضح الرسم البياني إحصائية فيرمي-ديراك عند الاتزان الحراري ودرجة حرارة (T) ثابتة، وكذلك حد ماكسويل-بولتزمان في الاتزان الحراري عند درجات الحرارة العالية والكثافات المنخفضة بحيث يمكن إهمال التأثيرات الكمية. من المهم أن نلاحظ أن إحصائية ماكسويل-بولتزمان تفترض عدم وجود تأثيرات بين الجسيمات في النظام وهذه حالة خاصة للغاز المثالي. لا يمكن تطبيق نظام ماكسويل - بولتزمان على درجات الحرارة المنخفضة، فإحصائية فيرمي-ديراك تصف بدقة نظام الفرميونات.
العدد الكلي للجسيمات: الإلكترونات (n) والثقوب (p) الموجودة في مستوي طاقة معيَّنة E
توزيع الإلكترونات وفقًا لطاقة حركتها
توزيع الثقوب وفقًا لطاقة حركتها
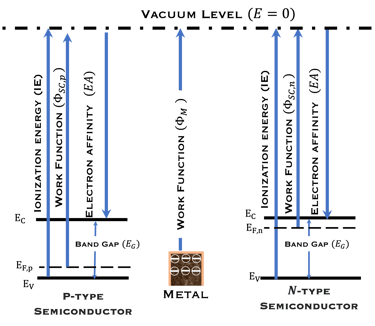
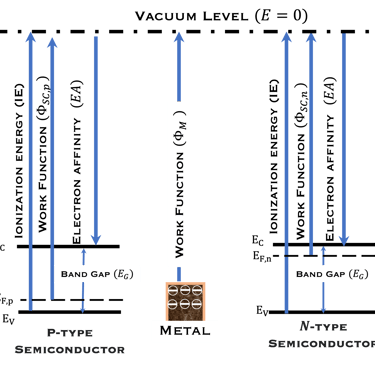
على اليمين: نموذج للإلكترونات الحرة لكثافة الحالة (DOS) مقابل الطاقة، وتوضح الصورة فجوة النطاق والمعادلات الرياضية لقيمة كثافة الحالة D(E) مقابل الطاقة لكل من الإلكترونات والفجوات. المركز في الوسط (أسفل): إحصائية فيرمي-ديراك لثلاث درجات حرارة مختلفة تنطبق على أشباه الموصلات (النوع N والنوع P). الوسط (أعلى): معايير مختلفة يجب تحسينها بدرجة كبيرة عند اختيار الأقطاب الكهربائية لتقسيم الماء . اليسار: رسم توضيحي لشبه موصل تحت تدفق فوتونات ذات طاقة أعلى أو مساوية لفجوة النطاق. يُظهر ضخ الإلكترون في نطاق التكافؤ إلى نطاق التوصيل تاركًا فجوة في نطاق التكافؤ. هذا يعني أن تدفق الفوتونات يترك كمية كبيرة من الفجوات في نطاق التكافؤ. تصف إحصائية فيرمي-ديراك بدقة نظام الفرميون. (نحيل القارئ إلى مقررات جامعة التعلم الافتراضي السابقة وإلى المراجع المذكورة في هذا الموقع الإلكتروني. .
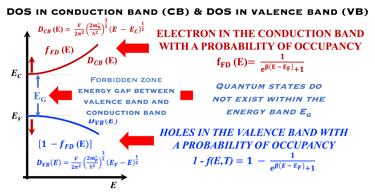
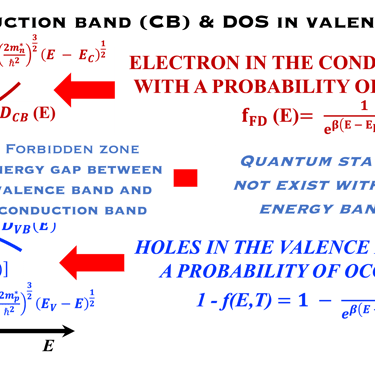
المعادلات الرياضية لإحصائيات ماكسويل-بولتزمان للإلكترونات والثقوب
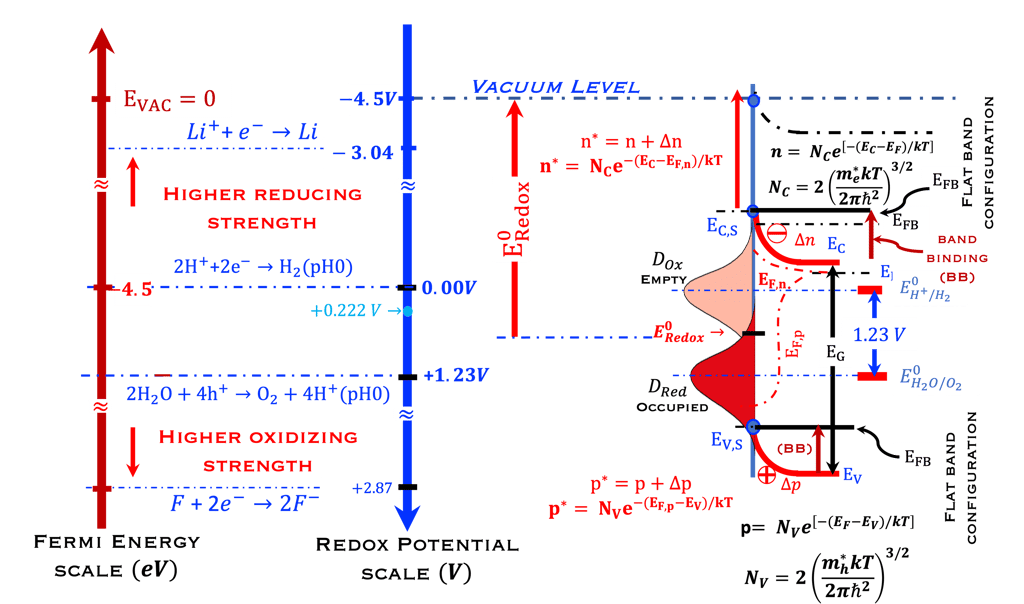
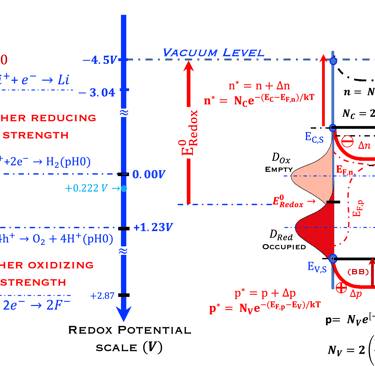
في الجزء الأيسر يوضح الرسم البياني أيضًا مقياسين للطاقة: المقياس الذي يستخدمه علماء الكيمياء الكهربائية بناءً على جهد الأكسدة والاختزال ( Redox potential Scale) بالمقارنة مع مقياس فيزيائيو الحالة الصلبة. يستخدم مقياس الفيزيائيين الإلكترون في الفراغ كمرجع (Fermi Energy Scale). أضفنا التفاعل الكهروكيميائي للماء في المحلول الحمضي، (0 فولت و1.23 فولت pH 0) وقارنا ذلك بأنظمة الأكسدة الأعلى (الفلور) والاختزال الأعلى ( الليثيوم)
في الرسم البياني، معلومات أخرى مهمة أيضاً مثل: الجهد الكهروكيميائي لحزم التكافؤ والتوصيل في الحالة الخاصة بالحزم المسطحة (Flat Band Potential) ومفهوم مستوى طاقة الأنواع المؤكسدة (فارغة) والمختزلة (ممتلئة) والتي تسمح برسم تشابه بين مستويات الطاقة في المادة الصلبة ومستويات الطاقة في نظام التحليل الكهربائي للأكسدة والاختزال
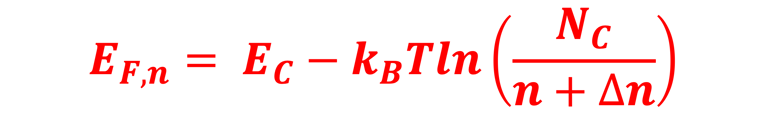
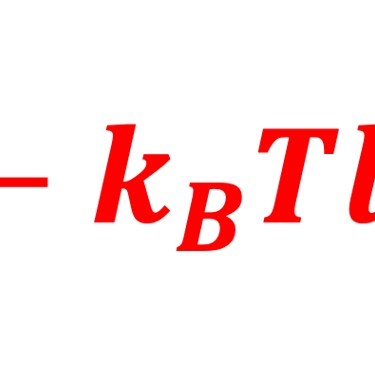


سؤال: يمكن للقارئ أن يحاول فهم السبب في أن مستوى فيرمي للإلكترونات في أشباه الموصِّلات (من النوع N) ينحرف قليلًا، في حين أن التغيُّر الرئيسي يكون في مستوى فيرمي للفجوات.
ننتقل إلى الجانب التجريبي والتذكير ببعض المفاهيم العلمية في الكميات الكهروكيميائية التي تعتبر ضرورية لفهم التفاعلات الكهروكيميائية الضوئية لإنتاج الهيدروجين الأخضر أو اختزال ثاني أكسيد الكربون


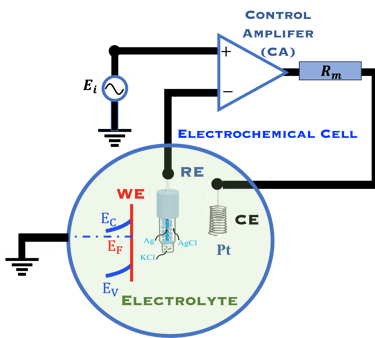
في مجال البحث والتطوير، تُعد القياسات الكهروكيميائية الضوئية الدقيقة ضرورية من أجل المقارنة مع الأقران الآخرين في مجال البحث والتطوير. يتطلب هذا استخدام نظامًا أو خلية كهروكيميائية مكونة من ثلاثة أقطاب (الرسم التوضيحي على اليمين): القطب العامل (WE)، وهو القطب شبه الموصِّل (النوع N) في الرسوم التوضيحية. القطب المعاكس (CE) الذي يسمح بمرور التيار الكهربائي من خلاله. نستخدم قطبًا ثالثًا لقياس الجهد الكهروكيميائي، تم تصميم هذا القطب بحيث يكون له جهد كهروكيميائي ثابت. يوضح الشكل هذه الخلية ونوعين من الأقطاب المرجعية (SHE و(Ag/Ag/Cl)، هذه الأقطاب الثلاثة متصلة ببعضها البعض إلكترونيًا عبر جهاز كهروكيميائي (Potentiostat/Galvanostat). يمكّن هذا النظام من التحكم بدقة عالية في الجهد الكهروكيميائي بين القطب العامل والقطب المرجع. وقياس التيار الناتج عن التفاعلات الكهروكيميائية في المحلول الإلكتروليتي وهو ما يقاس بين القطب المضاد (CE) والقطب العامل .
من المهم أن نشير أيضًا إلى أن الجهد الكهروكيميائي مقابل SHE لكل من تفاعل تطور الهيدروجين وتفاعل تطور الأكسجين يعتمد على الأس الهيدروجيني للمحلول، وسيتم مناقشة ذلك بناءً على معادلة نيرنست
القطب المرجعي الأكثر استخدامًا هو (Ag/AgCl) لأنه أسهل بكثير في التصنيع والصيانة، ويتكون من سلك فضي مغطى بطبقة رقيقة من من كلوريد الفضة (AgCl)، مغموس في محلول من كلوريد الكالسيوم (3M ؛ KCl)
القطب (Ag/AgCl) هو قطب مرجعي يستخدم على نطاق واسع كقطب مرجعي مفضل على الأقطاب المرجعية الأخرى نظرًا لانخفاض تكلفته وسهولة تحضيره، يتكون من سلك فضي مطلي بكلوريد الفضة ومغموس في محلول يحتوي على أيونات الكلوريد. يعمل القطب على أساس تفاعل الأكسدة والاختزال عند سطح القطب الكهربائي (Ag/AgCl) على النحو التالي: تُختزل أيونات الفضة إلى فلز الفضة عن طريق قبول إلكترون. من ناحية أخرى تتأكسد أيونات الكلور لتكوين غاز الكلور وتطلق إلكترونًا. يحافظ إطلاق أيونات الكلور في المحلول على التوازن الأيوني للمحلول.
من اليسار إلى اليمين: خلية كهروكيميائية زجاجية مزودة بثلاثة أقطاب كهربائية: قطب العمل (WE)؛ قطب مرجعي (RE)؛ قطب مضاد (CE). خلية كهروكيميائية مصنوعة من التفلون ذات جزأين يمكن ربطها بجسر مصممة لاستكشاف، على سبيل المثال، قطبين من أشباه الموصلات. خلية كهروكيميائية ضوئية واحدة مصنوعة من التفلون، مع نافذة للإضاءة
القطب المرجعي للهيدروجين (SHE): يتكون من سلك بلاتيني ذي مساحة سطح عالية مغمور في محلول حمضي حتوي على بروتونات وغاز الهيدروجين (activity 1). لإبقاء محتوى الهيدروجين في حالة مستقرة، يتم ضخ غاز الهيدروجين ليتدفق عبر المحلول الداخلي (كما هو موضح في الرسم التخطيطي). يعتمد جهد القطب على تركيز البروتون والضغط الجزئي للهيدروجين. تفاعل القطب الكهربائي وجهد القطب (معادلة نيرنست)
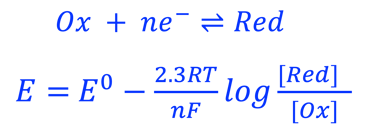
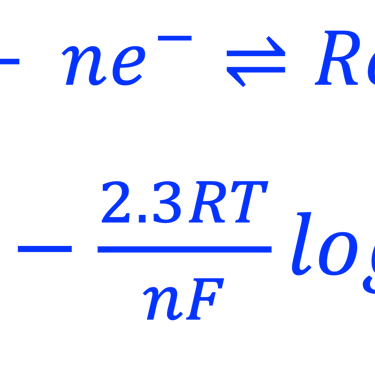
خلفية عامة عن معادلة نيرنست
لا يمكن قياس جهد كهروكيميائي بشكل مباش، ولكن فقط بالنسبة إلى قطب مرجعي ويتم اختيار القطب المرجعي كنقطة صفر للجهد الكهروكيميائي. فقطب الهيدروجيني القياسي (SHE) هو أساس المقياس الديناميكي الحراري في الكيمياء الكهربائية ويمكن مقارنتها بجميع المقاييس الأخرى القائمة على تفاعلات كهروكيميائية أخرى مثل الفضة في حالة توازن مع كلوريد الفضة (Ag/AgCl). ويبلغ جهد نصف الخلية لقطب (Ag/AgCl) تقريبًا 0.197V فولت مقابل قطب الهيدروجين القياسي (SHE) عند درجة حرارة 25 درجة مئوية . مصادر المعلومات: ويكيبيديا XYZ...


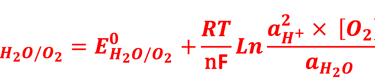

معادلة نيرنست للقطب (-)
معادلة نيرنست للقطب (+)
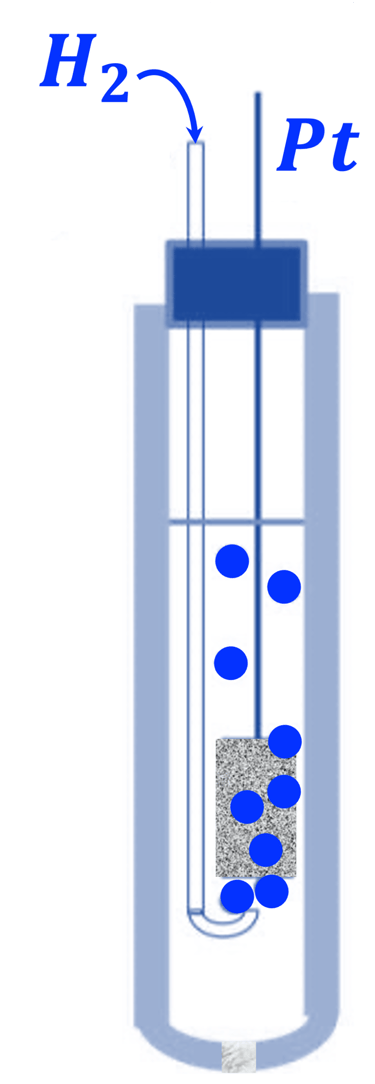
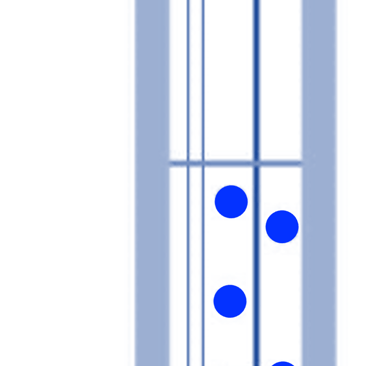
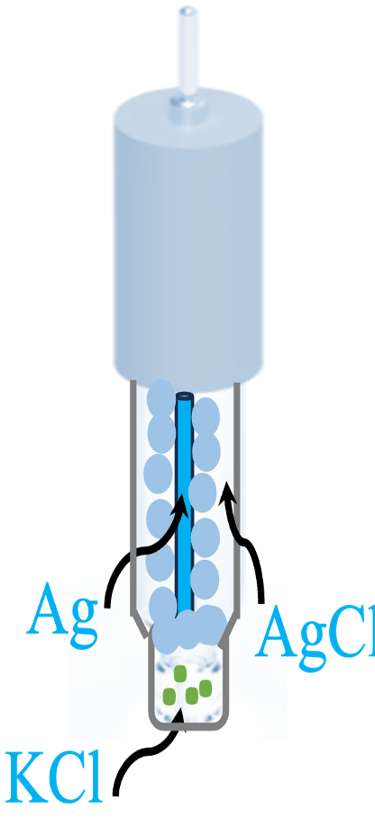
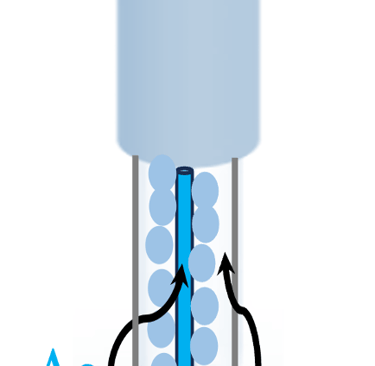




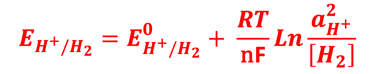
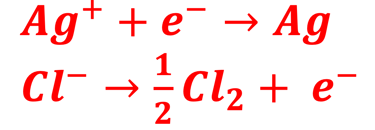
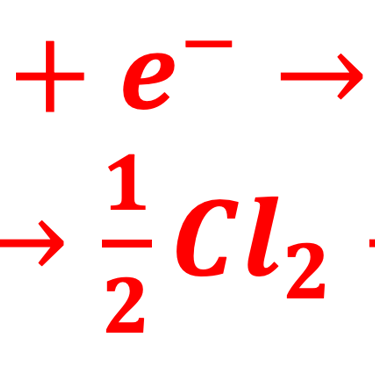
"فريت" لتجنب تسريب محلول الإلكتروليت من القطب المرجعي والحفاظ على التلامس الكهربائي

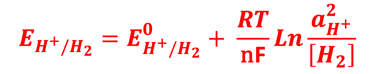
معادلة نيرنست لانقسام الماء
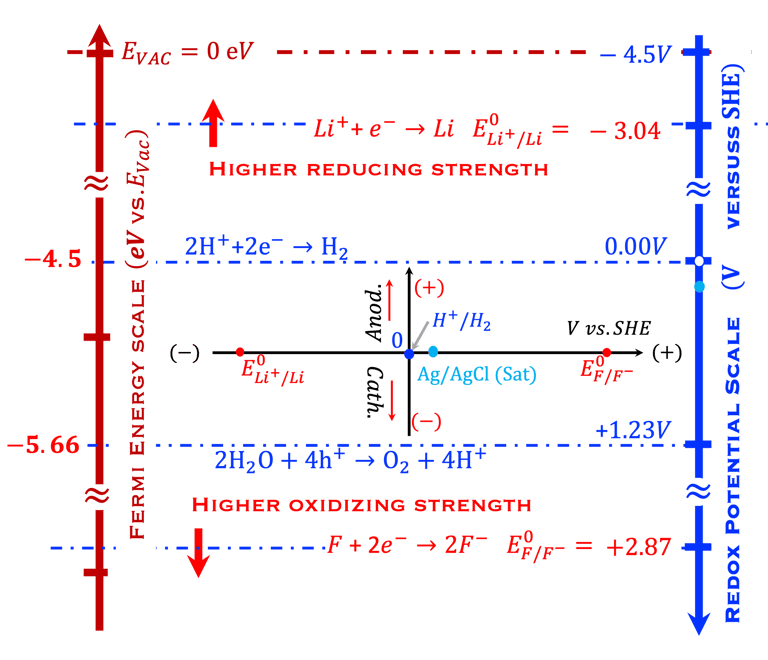
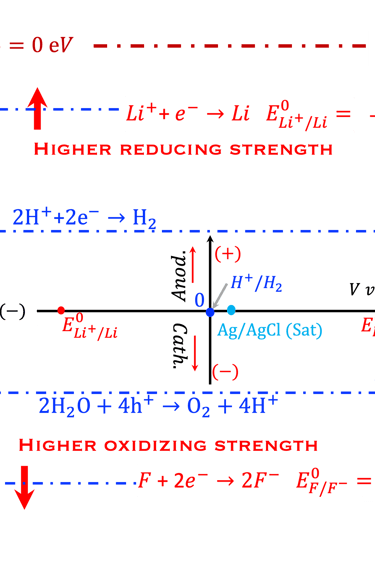
الجانب الأيمن في الرسم التوضيحي أعلاه: الجهد في العمودي-Y (باللون الأزرق) للتعبير عن الجهد الكهربائي بالفولت مقابل قطب الهيدروجين (Volt vs. SHE)
الجانب الأيسر في الرسم التوضيحي أعلاه: المقياس لطاقة الإلكترون مقابل الفراغ (eV vs. Vacuum). لتوفير أدوات لكل من فيزيائيي الحالة الصلبة وعلماء الكيمياء الكهربائية وكذلك علماء الكيمياء الكهربائية وكذلك المهندسين من أجل فهم بعضهم البعض في مصطلح القياسات. في الواقع, يبني الكهروكيميائيون قياساتهم على قطب المرجعي هيدروجيني (SHE). على سبيل المثال بالنسبة لمحلول حمضي (pH0)، يحدث اختزال البروتونات بجهد يساوي 0.00 فولت، ويتم تأكسد الماء بجهد 1.23 فولت (vs. SHE). غالبًا ما يستخدم الفيزيائيون مستوى الطاقة كمرجع (E in eV vs. Vacuum)
لقد وضعنا أيضًا بعض أنظمة الأكسدة والاختزال: أنظمة تحلل الماء (للرقم الهيدروجيني الحمضي المتوسط0) وأنظمة الأكسدة والاختزال الأخرى الأكثر تأكسدًا واختزالًا. كما تم رسم المحورين (X و Y) المستخدمين في القياسات الكهروكيميائية للمقارنة (وسط المخطط) بما في ذلك اتجاه التيار الأنودي والكاثودي، والجهد الكهروكيميائي لـ (SHE) و (Ag/Ag/Cl)
نريد أن نقرّب القارئ من تقنيات القياس في الكيمياء الكهربائية والكيمياء الكهربائية الضوئية أكثر من أي وقت مضى، ولذلك، نوضح هنا في هذا الرسم التوضيحي أدناه
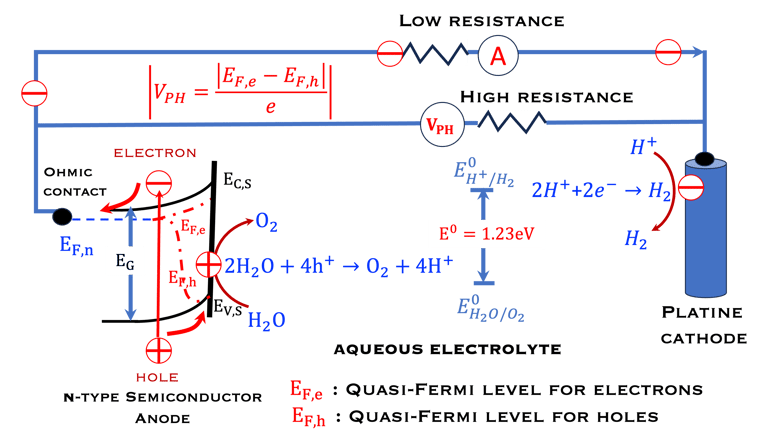
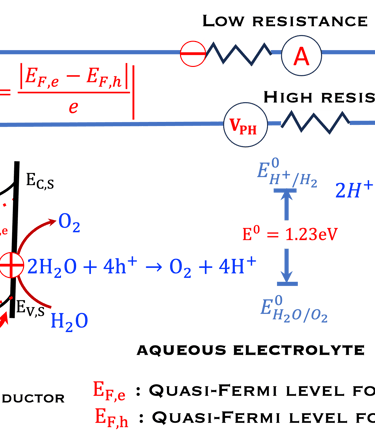
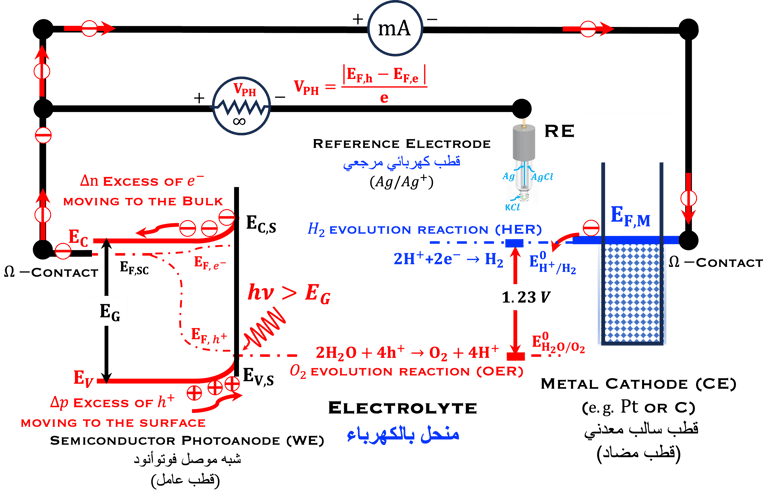
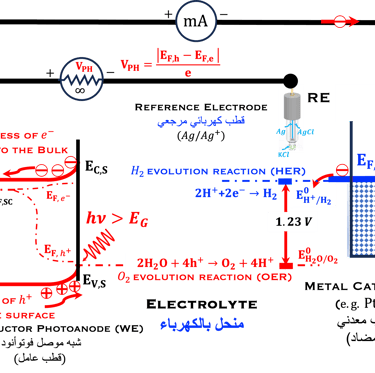
نعرض هنا خلية كهروكيميائية ضوئية ذات قطبين يمر من خلالها تيار ضوئي بين القطب العامل (WE) والقطب المضاد (CE). القطب العامل (WE) هو شبه موصِّل (من النوع N) مُعرَّض للإضاءة، وقد سبق أن شرحنا سبب انقسام المستوى الفرمي إلى مستوى شبه فرمي للإلكترونات ومستوى شبه فرمي للثقوب وهذا يؤدي إلى إنشاء الحد الأقصى للجهد الضوئي وهو انقسام مستويات الفيرمي لحاملي الشحنتين
هنا، النظام الكهروكيميائي الأكثر استخدامًا في البحث والتطوير؛ الخلية الكهروكيميائية الضوئية ثلاثية الأقطاب. ويمر التيار بين القطب العامل شبه الموصِّل (من النوع N) شبه الموصِّل (WE المعرض للإضاءة) والقطب المضاد (CE). يتم قياس الجهد الكهربي هنا مقابل القطب المرجعي (Ag/AgCl). على غرار الرسم التوضيحي أعلاه، أظهرنا طاقة شبه فيرمي لكل من الإلكترونات والثقب التي تحدث من الشحنة الزائدة عند إضاءة المصعد.
في الحالات المذكورة أعلاه (الأنظمة ثنائية القطب وثلاثية القطب)، اخترنا قطبًا موجبًا شبه موصل مناسبًا، فيما يتعلق بجهد الأكسدة والاختزال الكهروكيميائي (الطاقة) المناسب لتقسيم الماء. هذا هو أحد التحديات في البحث والتطوير للعثور على المواد المناسبة للأقطاب الكهربائية
الملاحظة الأولى: الحد الأقصى للجهد الكهروكيميائي الضوئي الذي يمكن قياسه باستخدام الفولتميتر


الملاحظة الثانية: تحتوي الخلية ذات القطبين على مهبط (CATHODE) ومصعد (ANODE)، ولا يمكن قياس المساهمات الفردية للكاثود والأنود في جهد الخلية. جهد الخلية يساوي

الملاحظة الثالثة: تتيح الخلية ثلاثية الأقطاب التي تحتوي على قطب كهربائي مرجعي (بجهد كهروكيميائي ثابت ومعروف) إمكانية تحديد جهد القطبين الكاثود والأنود مقابل جهد القطب المرجعي، وهكذا يتكون جهد الخلية من الفرق بين جهدين تم قياس كل منهما مقابل الجهد الكهربي المرجعي (RE)




الملاحظة الرابعة: عند إجراء بحوث الكيمياء الكهروكيميائية، من الضروري قياس الجهد الكهروكيميائي مقابل قطب مرجعي ثابت (RE)، وإقامة علاقة مع دالة العمل ومستوى فيرمي مقابل طاقة مستوى الفراغ للنظام الكهروكيميائي الضوئي. لذا من المهم أن تكون على دراية بكلا المقياسين: المقياس الكهروكيميائي ومقياس مستوى فيرمي.
في الجدول أدناه، نعرض قائمة واسعة من التفاعلات النصفية على شكل اختزال وجهدها الكهروكيميائي (وليس تفاعلات أكسدة؛ هذه هي القاعدة المُستخدمة). وبالتالي، يُمكن قياس فرق الجهد بين طاقة الإلكترونات بين الكاثود والأنود مباشرةً من خلال هذا الجدول. على سبيل المثال، تفاعلات الأكسدة والاختزال للماء.
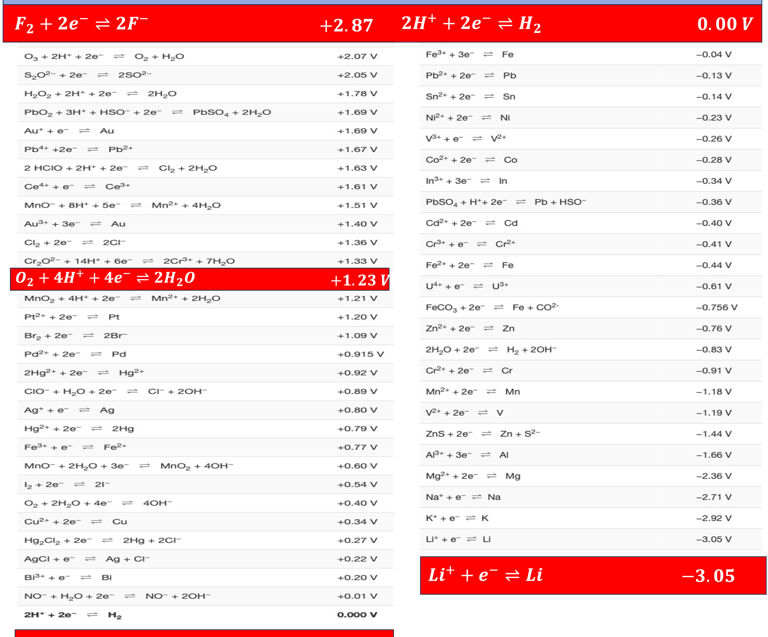
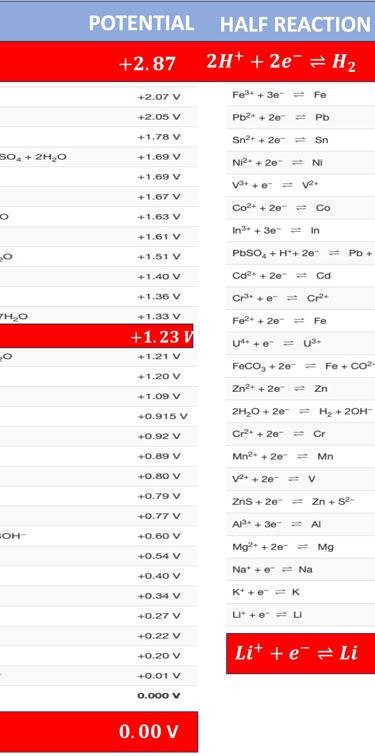
اختزال أيون الهيدروجين
أكسدة الماء
التفاعل الكلي
ضع في اعتبارك أن جرامًا واحدًا من غاز الهيدروجين يتطلب (96500C) في الدقيقة (1min)، سيسمح لنا ثابت فاراداي (F) بالانتقال من كمية الإلكترونات في المول إلى الشحنة الحالية المنقولة:
إذا انتقل في التفاعل الكهروكيميائي عدد n من الإلكترونات في التفاعل الكهروكيميائي، فإن الشحنة الكلية لكل مول، Q
تُظهر هذه العملية الحسابية البسيطة أنه لإنتاج 1 جم من الهيدروجين في دقيقة واحدة (60 ثانية) عن طريق الاختزال الكهروكيميائي لبروتونات الهيدروجين نحتاج إلى تيار لا يقل عن (1610A). الأمبير الواحد يكافئ تدفُّق كولوم واحد (1C) لكل ثانية (60s)
بعض المعلومات الأساسية حول الجانب الديناميكي الحراري للتفاعل غير التلقائي
انقسام الماء هو تفاعل ماص للحرارة حيث أن التغير في الطاقة الحرة لإنتاج الهيدروجين والأكسجين كمية موجب. في الظروف القياسية أي ( 298 كلفن و1 مول/لتر و1 بار) سيكون سيكون التغيُّر في الطاقة الحرة لتحويل الماء إلى هيدروجين وأكسجين: 237 كيلوجول لكل مول. من المعادلة أعلاه للطاقة الحرة، إذا كانت ΔG موجبة، فلا بد أن تكون TΔS سالبة، وهو ما يعني أن ΔS سالبة. ومن ثَمَّ إنقسام الماء إلى أكسجين وهيدروجين يتطلب إمدادات طاقة، مثل الحرارة أو الضوء أو الكهرباء.
نظريًا، التغير في طاقة جيبس الحرة يساوي 237 كيلوجول لكل مول، والتغير في المحتوى الحراري يساوي 285.8 كيلوجول لكل مول، والطاقة الحرارية تساوي 48.7 كيلوجول لكل مول. هذا يشير إلى أن انقسام مول واحد من الماء السائل لإنتاج مول واحد من الهيدروجين في ظل الظروف القياسية يتطلب طاقة إجمالية نظرية: 285.8 كيلو جول بما في ذلك 237.1 كيلو جول من الكهرباء و 48.7 كيلو جول من الحرارة. الجهد المرتبط بتغير المحتوى الحراري (Enthalpy) يُعرف باسم الجهد "المحايد حراريًا" (thermoneutral voltage). من معادلة الطاقة الحرة والعلاقة مع الإنتروبي والإنثالبي بالانتروبي والإنثالبي نستنتج ما يلي: إذا كانت ΔG موجبة، فلا بد أن تكون TΔS سالبة، وهو ما يعني أن ΔS سالبة. ومن ثَمَّ إنقسام الماء إلى أكسجين وهيدروجين يتطلب إمدادات طاقة، مثل الحرارة أو الضوء أو الكهرباء.

لنفترض أننا حققنا وضعًا مثاليًا للمُحلِّل الكهربائي بكفاءة 100%، حيث يسمح جهد 1.48 فولت بتقسيم الماء في ظل ظروف قياسية، فإن الحرارة المتولدة منه تساوي الحرارة اللازمة للتحليل الكهربائي، أي حالة "محايدة حراريًا". وبالتالي يمكننا القول: المُحلِّل الكهربائي لا يُطلق ولا يمتص حرارةً من البيئة المحيطة. إذا كان الجهد أقل من جهد الخلية البالغ 1.48 فولت (لكن أعلى من 1.23 فولت)، فإن المُحلِّل الكهربائي يمتص الحرارة باستمرار من البيئة المحيطة. أما إذا كان الجهد أعلى من 1.48 فولت، فإن النظام يُولِّد حرارةً زائدةً ويجب إزالة الحرارة الزائدة لضمان عمل الخلية بدرجة حرارة متساوية. تُعدّ إزالة الحرارة ميزة هندسية أساسية في تصميم أجهزة التحليل الكهربائي للماء، هذا يقودنا إلى تحدٍ تكنولوجي حاسم: جميع المحللات الكهربائية التي نستكشفها هنا تعمل عند درجات حرارة أقل من 100 درجة مئوية، ويعتمد الحد الأقصى لدرجة الحرارة على استقرار الأغشية. كذلك، فإن الجهد أعلى بكثير من 1.48 فولت، وبالتالي فإن إزالة الحرارة هي ميزة هندسية أساسية في تصميم أجهزة التحليل الكهربائي للمياه. وتوجد تحديات أخرى، وتحديدًا "الجهد الزائد" (Overpotential) للتفاعل الكهروكيميائي لإنتاج الهيدروجين على المهبط، والتفاعل الكهروكيميائي لإنتاج الأكسجين على المصعد. يجب التغلب على "الجهد الزائد" باستخدام محفزات كهربائية فعالة، وتحسين الإلكتروليت من حيث عناصر الأكسدة والاختزال، وتحسين متفاعلات "نقل الكتلة"
عدد الإلكترونات المتبادلة لمول واحد من الماء: n = 2 وثابت فاراداي (96 500 C/mol). هناك علاقة مباشرة بين الجهد الكهروكيميائي والطاقة الحرة . نظريًا، التغير في طاقة جيبس الحرة يساوي 237 كيلوجول لكل مول
الشحنة الكلية ل 1 مول من الإلكترونات - 96485 كولوم
التغير في طاقة جيبس الحرة يساوي 237 كيلوجول لكل مول، هذا التفاعل غير تلقائي من الناحية الديناميكية الحرارية
يمكننا تخيل نظام لتحلية المياه، وضخ المياه باستخدام الطاقة الشمسية و/أو طاقة الرياح إلى جانب وحدات التحليل الكهربائي لإنتاج الهيدروجين الأخضر. من المهم ملاحظة أن الماء المستخدم في التحليل الكهربائي يجب التحكم فيه جيدًا من حيث النقاء والتركيب ودرجة الحموضة لحقنه بشكل مناسب إلى الأنود حيث يتم تقسيمه إلى أكسجين وبروتونات هيدروجين وإلكترونات سالبة. نظام المحللات الكهربائية مُصمم لنقل البروتونات عبر غشاء موصل للبروتونات لكي تصل إلى المهبط، في حين تتحرّك الإلكترونات من الأنود عبر دائرة الكهربائية الخارجية مدفوعة بالجهد (جهد الخلية). هكذا، تتفاعل البروتونات والإلكترونات لإنتاج الهيدروجين في المهبط. نعطي هنا التفاعلات الكهروكيميائية حيث يعتمد جهد الأكسدة والاختزال على درجة الحموضة للإلكتروليت
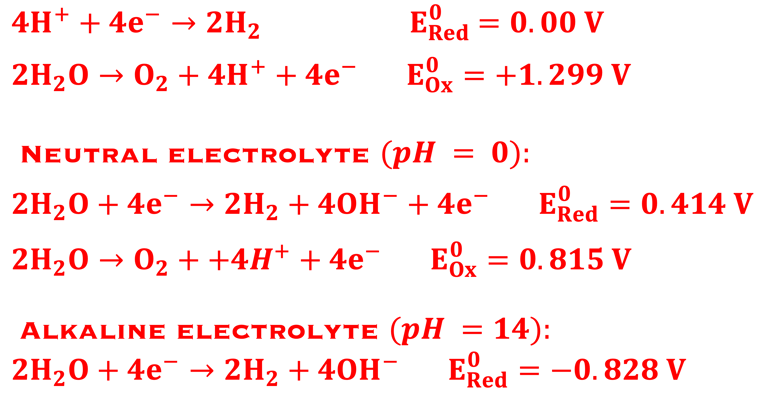


التفاعل الشامل لانقسام الماء
الطاقة المطلوبة لتنشيط التفاعل الكيميائي
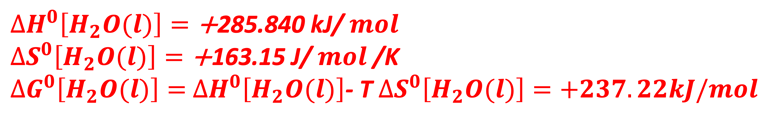
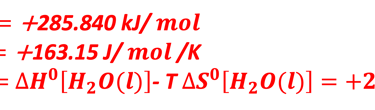
Sources used here: Electrochemical Power Fundamentals, Systems, and Applications Hydrogen Production by Water Electrolysis // Edited by Tom Smolinka Fraunhofer Institute for Solar Energy Systems ISE, Freiburg, Germany and Juergen Garche Ulm University, Ulm, Germany // as well as Roel van de Krol l Michael Gra ̈tzel Editors, Photoelectrochemical Hydrogen Production: Basic Principles S. Shiva Kumar, V. Himabindu, Materials Science for Energy Technologies 2 (2019) 442–454 // Wei Li et al. Mater. Adv., 2022, 3, 5598–5644
هنا، نلقي نظرة على تقنية كهروكيميائية تُستخدم لقياس ديناميكيات عمليات الأكسدة والاختزال. التقنية التي تعتمد عن تطبيق نطاق جهد محدد وقياس التيار الناتج عن تفاعلات الأكسدة والاختزال أو التآكل أو العمليات الأخرى التي تحدث على سطح الأنود والكاثود. نصف الاستجابة الطيفية (Spectral response) وكيفية استنتاج الكفاءة الكمية والكفاءة لإنتاج الهيدروجين (Power to Hydrogen). هذه التقنيات الكهروكيميائية تمكّن من تحديد ما إذا كانت الخلية الكهروكيميائية الضوئية تفي بمواصفات الأداء والجودة، وتحديد أي عيوب تحتاج إلى معالجة للمضي قدمًا نحو إثبات المفهوم


الكروماتوجراف الغازي (gas chromatograph) هو جهاز يقوم بالتحليل الكمي والنوعي. يتم حقن العينات الغازية بواسطة صمامات الحقن الآلي
صندوق أسود لمنع الضوء الشارد، وفي الوقت نفسه يعمل كقفص فاراداي لمنع الشحنات الكهربائية من المجالات الكهربائية الخارجية من اختراق القفص
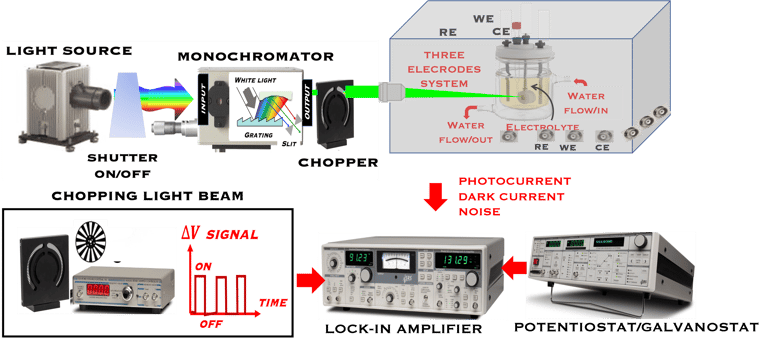
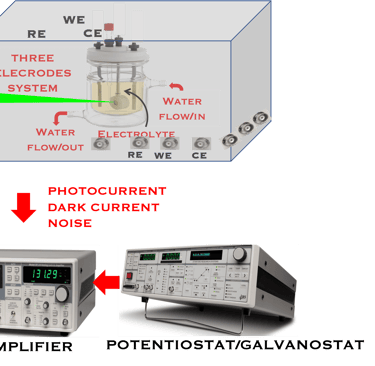
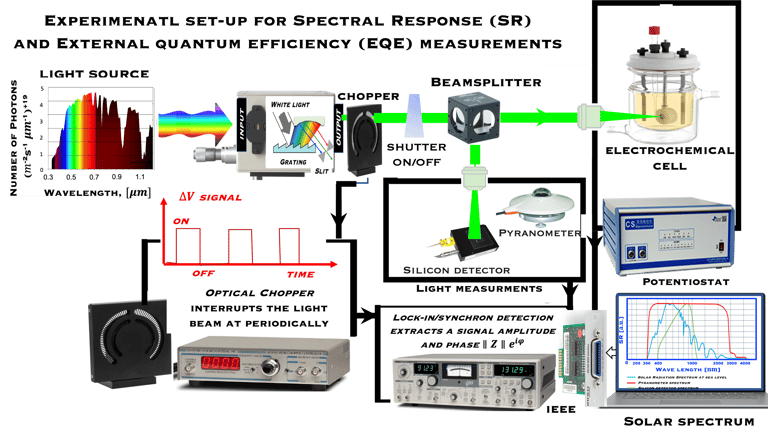
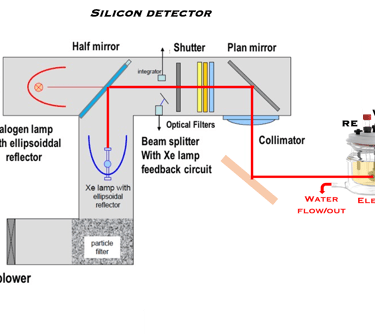
يوضح الشكل مجموعة تجريبية تسمح بالحصول على ضوء أحادي اللون، وتتكون من مصدر ضوء،(Hal-W lamp) ومطياف ضوئي (Monochromator)، ونظام لقطع الضوء بشكل دوري (Chopper). يتم إرسال الضوء أحادي اللون الذي تم الحصول عليه إلى قطب كهربائي شبه موصل (من النوع N)
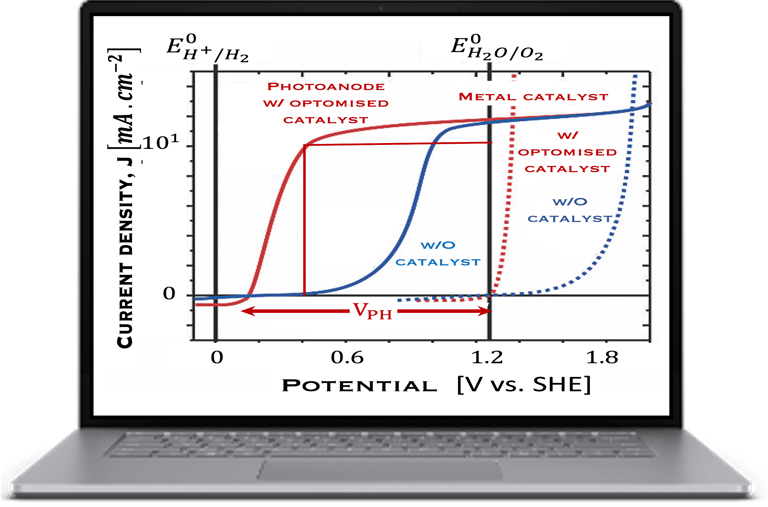
يمكن تصنيع مخططات مجموعة الأجهزة المذكورة أعلاه بالكامل، ولكن هناك مجموعة متاحة تجاريًا. هذا النظام مُناسب تمامًا لمختبرات الأبحاث، وللقياس والتحليل الكهروكيميائي، بما في ذلك التآكل والبطاريات وأجهزة الاستشعار وعلوم الحياة والكيمياء البيئية. تطبيق جهد كهربائي (Potentiostatic mode) أو حقن تيار كهربائي (Galvanostatic mode) طريقتان لدراسة العملية الكهروكيميائية. يعد قياس الجهد الدوري (Cyclic Voltametry)، الطريقة الأكثر استخداماً في التحليل الكهروكيميائي ووسيلة لفهم عميق لمواد القطب الكهربائي والمحفزات وأشباه الموصلات الجديدة ذات الإمكانات الأكبر لتحويل الطاقة الشمسية وتقسيم الماء و/أو اختزال ثاني أكسيد الكربون. في مثل هذه التجارب يتم تطبيق نطاق من الجهد، على سبيل المثال من -V إلى +V بمعدل مسح خطي (mV/s). ويتم قياس التيار في ذلك الظلام وتحت إضاءة كل قطب كهروكيميائية الناتج عن الأكسدة والاختزال. يتم استخدام برنامج محاكاة وخوارزميات للتحكم في التجارب وملاءمة المنحنيات (I-V)، لفهم التفاعلات الكهروكيميائية المختلفة، مثل إنتاج الهيدروجين، والاختزال الكهروكيميائي لثاني أكسيد الكربون.


الكابل المحوري
تأثير المحفزات في نقل الإلكترونات بين القطب والمتفاعلات وتسهيل التفاعلات الكهروكيميائية سواء أثناء إضاءة القطب وبدون إضاءة أيضًا في القياسات الكهروكيميائية. على الجانب الأيمن، يُظهر الرسم التخطيطي نوعيًا بوضوح تأثير المحفزات على عامل التعبئة (Fill Factor) و I(V). نعرض هنا خلية كهروضوئية كيميائية ذات قطب موجب (نوع N) وقطب سالب معدني (كاثود)
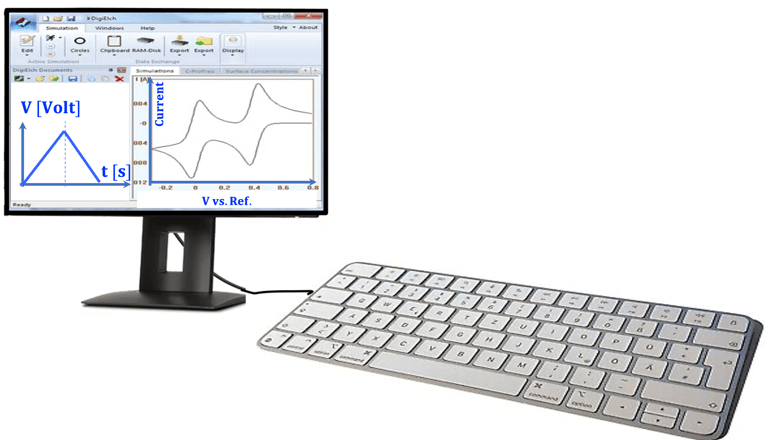
تُمكّن مجموعة الأجهزة هنا من اختبار قدرة القطب شبه الموصل على امتصاص أقصى نسبة من الضوء المُشعّ بكفاءة ضمن نطاق مناسب من الأطوال الموجية. الكفاءة الكمومية هي المقياس الذي يعكس كفاءة نظام التحفيز الضوئي في تحويل الفوتونات الممتصة إلى تيار ضوئي

نقطة مهمة، إذ نراقب الجهد المطبق بمعدلات مسح خطية مختلفة (V vs. t)، كما هو موضح على الجانب الأيسر من الشاشة. التيار الكهربائي مرتبط بالتفاعلات الكهروكيميائية التي تحدث على الأقطاب الكهربائية، كما هو موضح على الجانب الأيمن من الشاشة (Current,I vs. V). يتيح لك تطبيق (Curve Fitter) قياس الشحنة المستهلكة في التفاعلات الكهروكيميائية واستنتاج طبيعة هذه التفاعلات الكيميائية.
التحكم في الجهد الكهروكيميائي المطبق على القطب العامل مقابل مرجع، بما في ذلك القياس الدقيق للتيار الناتج المنسوب إلى تفاعلات الأكسدة والاختزال الكهروكيميائية أو التفاعلات الأخرى، مثل تآكل الأقطاب الكهربائية، هو أحد أهم وظائف مجموعة الأجهزة المسماة (Potentiostat)
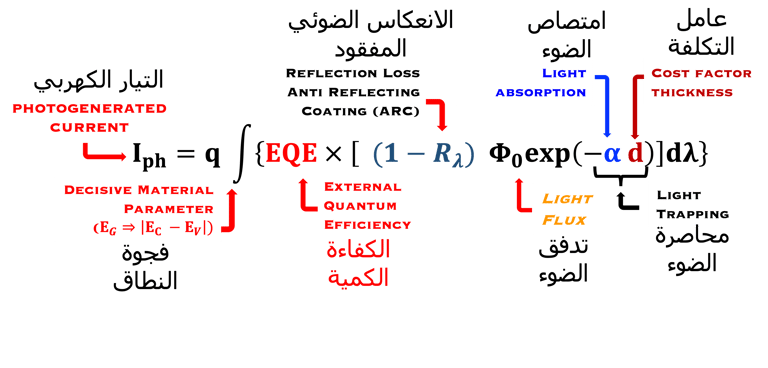
نقدم هنا بعض المعادلات الرياضية حول الاستجابة الطيفية (SR) والكفاءة الكمية (QE) والكفاءة الكهروكيميائية (.EFF). وسنربط بين القياسات أي ما هو تجريبي والمعادلة الرياضية. وسنناقش طريقة تحقيق أفضل النتائج من حيث الكفاءة في الكيمياء الكهروكيميائية الضوئية (تحويل الطاقة إلى هيدروجين)
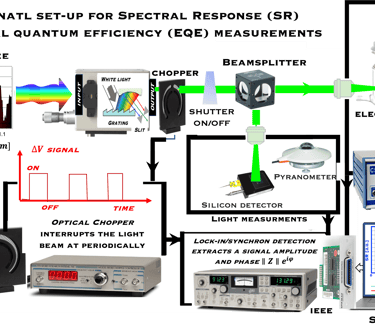
هناك علاقة بين سرعة الضوء والطول الموجي، هذه المعادلة المهمة معروفة باسم علاقة بلانك
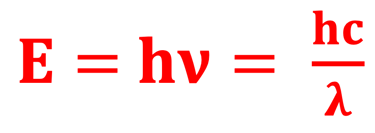
ثابت بلانك
سرعة الضوء
طول الموجة الضوئية
ماذا تعني هذه المعادلة ؟ الفوتون له خواص موجية وخواص جسيمية في آن واحد. وكلما زاد الطول الموجي للفوتون، تقل الطاقة والعكس صحيح، بينما كلما زاد التردد، زادت الطاقة والعكس صحيح
التردد
الطاقة
يُظهر الفوتون سلوكًا موجيًا في بعض التجارب مثل التداخل البصري، وهو نوع من الظواهر الطبيعية التي تحدث عندما تندمج موجتان ضوئيتان. وفي بعض البعض الآخر، يتصرف الفوتون كجسيم له طاقة E، ويتفاعل مع المادة عن طريق نقل كمية معينة من الطاقة مثل التأثير الكهروضوئي هو عملية توليد الجهد أو التيار في الخلية الكهروضوئية والكهروكيميائية الضوئية. كما هو موضح أعلاه أصغر قَدْر من الطاقة يمكن تبادله مع المادة يساوي ثابت بلانك × تردد الفوتون
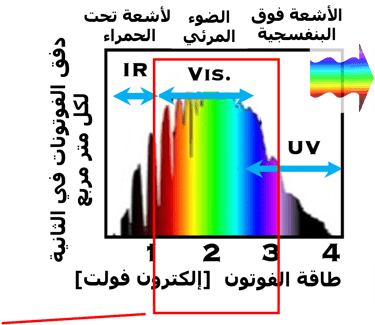
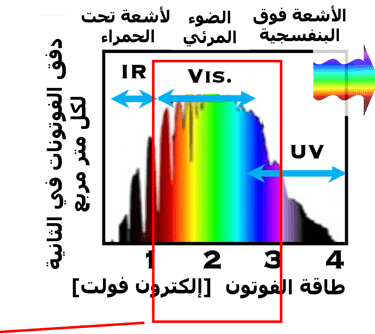
هنا عدد الفوتونات الساقطة على سطح القطب شبه الموصِّل (من النوع N)

بناءً على مفهوم أن فوتونًا واحدًا يولد إلكترونًا واحدًا وبعض الإلكترونات المتولدة ضوئيًا يمكن أن تشارك في التيار الضوئي يمكننا قياس شدة التيار في الخلية أثناء إضاءة القطب شبه الموصِّل (المصعد) على شحنة الإلكترون ثم نقسم قيمة شدة التيار على شحنة الإلكترون


الكفاءة الكمية الخارجية سوف تعطيك معلومات عن عدد الإلكترونات الناتجة عن تدفق الفوتونات الساقطة والتي أنتجت التيار الضوئي. الكفاءة. الكفاءة الكمية الخارجية (EQE) يعبر عنها كنسبة مئوية
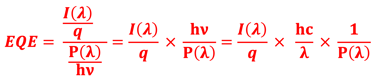
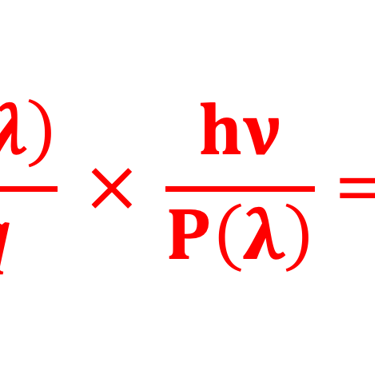
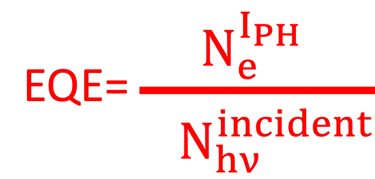
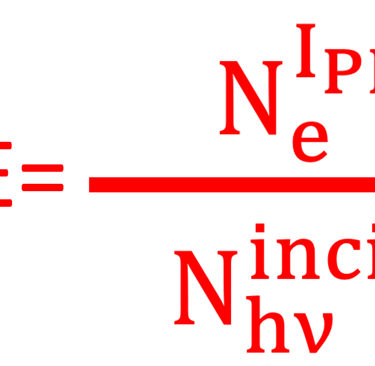
الإجراءات التجريبية
تُنسب كل 𝝀 [نانومتر] إلى طاقة E = 𝒉𝒄/( 𝝀)
قياس طيف الضوء: P(𝝀)
قياس التيار الضوئي للخلية الشمسية: I(𝝀)
حساب النسبة: P(𝝀) / I(𝝀) أي SR(𝝀)
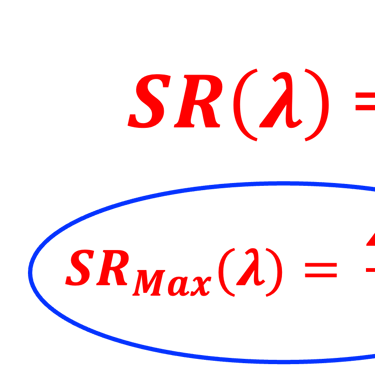
استخدام العلاقة الحسابية بين SR(λ) و EQE(λ)
SR(λ) is the spectral response of the device
هي الاستجابة الطيفية للجهاز SR(λ)
الخطوات المهمة للتجارب الخاصة بقياس (𝝀)SR و (𝝀)EQE باستخدام هذه المجموعة من الأجهزة
من الواضح أن اختيار جهاز قياس كمية أو شدة الضوء لتحديد كمية الضوء المرئي فوق البنفسجي وتحت الأحمر هي المهمة الأولى التي يجب القيام بها، ويعتمد على النطاق الطيفي الذي يالذي يستجيب له النظام الكهروكيميائي الضوئي المراد دراسته وهذا يرتبط بـامتصاص الضوء الذي يرتبط ارتباطًا وثيقًا بـفجوة نطاق أشباه الموصلات لمادة الأقطاب الكهربائية. تتأثر دقة القياسات ببعض الظروف البيئية، وأهمها: 1- الإضاءة الخارجية غير المرغوبة التي تجعل القياس خاطئ وغير دقيق. هناك أيضًا درجة الحرارة التي قد تؤدي إلى تغيير في خصائص الجهاز المستخدم وتؤثر أيضًا على دقة القراءة.
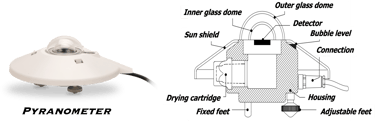
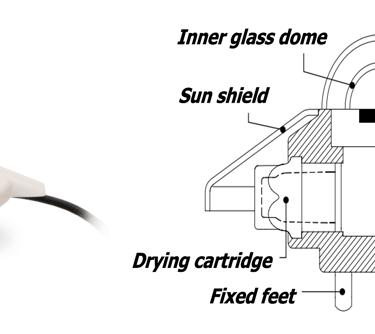
1) أفضل جهاز لقياس كمية الإشعاع الكلي هو ما يسمى: البيرانومتر (Pyranometer). ويُستخدم هذا غالبًا في علم الأرصاد الجوية لقياس كمية الإشعاع الشمسي الكلي الذي يصل إلى الأرض مباشرة أو بشكل غير مباشر . يعتمد البيرومتر، كما يوحي اسمه، على التأثير الكهرو-حراري (يُعرف باسم تأثير سيبيك)
2) هناك أجهزة أخرى أو كاشفات ضوئية، أبسطها يعمل على نفس مبدأ الخلايا الكهروضوئية ويحول الضوء مباشرة إلى كهرباء. وتعتمد على مواد شبه موصلة، مثل السيليكون، كمستشعر للضوء المرئي والأشعة تحت الحمراء. هناك كاشفات أخرى تعتمد على عدة مواد شبه موصلة ذات فجوة نطاق مختلفة لتوسيع الحساسية الطيفية
3) المصابيح لإضاءة القطب ينبغي أن توفر ضوءاً أبيض ثابتاً ومستقراً بشكل جيد ينتج طيفاً مماثلاً أو قريباً من طيف الشمس.
3) متاحة تجاريا: هنا مصدر محاكاة الشمس الذي يتيح الحصول على ظروف AM1.5؛ 1000 واط لكل متر مربع)
5) يمكن استخلاص الكثير من المعلومات من الاستجابة الطيفية، وأهمها قيمة فجوة النطاق ونطاق الطاقة (وأطوال الموجات) التي تكشف عن الحساسية الضوئية للخلية الكهروكيميائية
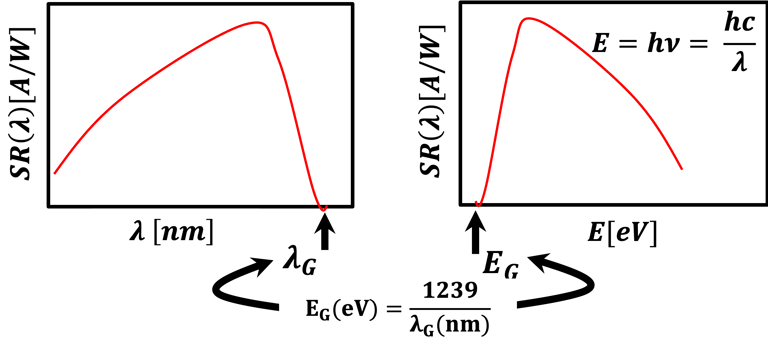
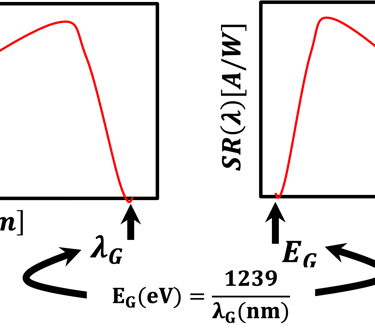
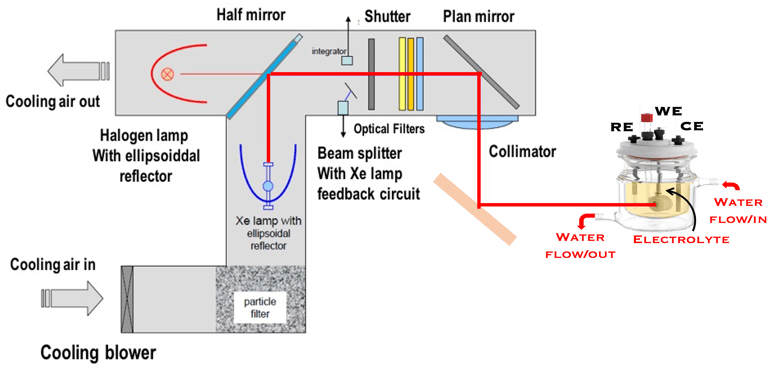

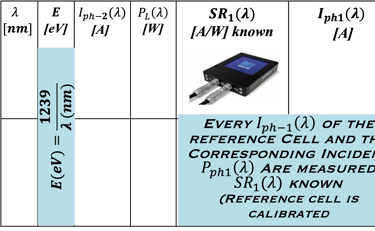
يوضح الجدول أدناه أفضل طريقة ملاءمة تعتمد على قياسات التيارات الضوئية واستخدام معادلة الرياضيات لحساب (λ)SR
1) قياس الخلية المرجعية SR1(λ) (جهاز سيليكون، متاح تجاريًا وبيانات التحويل المرجعية (W/A) المعروفة)
2) قياس التيار الضوئي للخلية الكهروكيميائية (القطب الموجب تحت الإضاءة، نحافظ على نفس ظروف الإضاءة
يمكن استنتاج الاستجابة الطيفية للخلية الكهروكيميائية (المعادلة الرياضية في الجدول)
الكفاءة الكمية (EQE) لها أهمية خاصة في تحديد التيار الذي ينتجه الجهاز (خلية شمسية صلبة، خلية كهروكيميائية) عند تعرضه للإشعاع بواسطة فوتونات ذات طول موجي معين
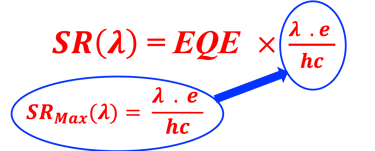
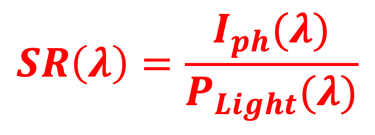
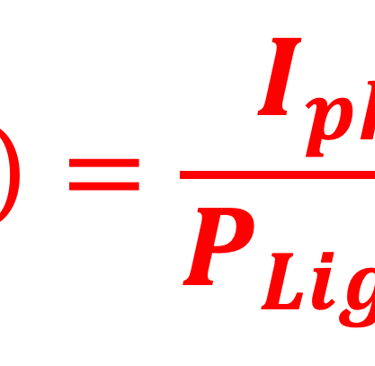
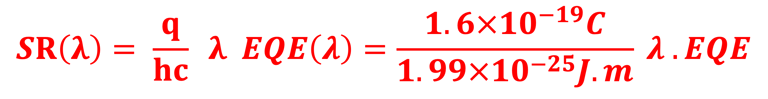
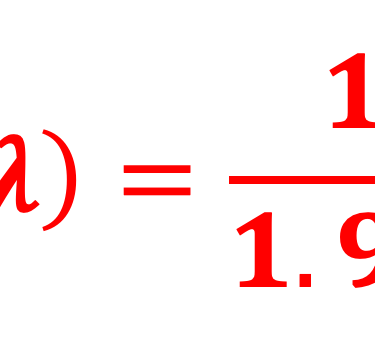
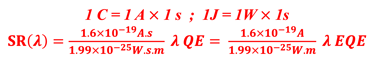
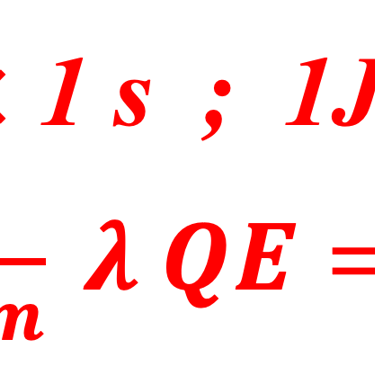
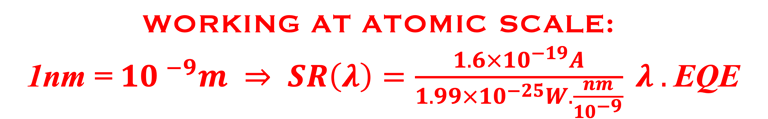
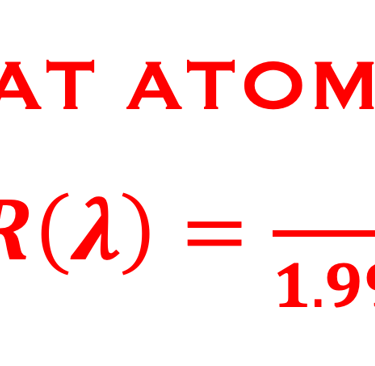
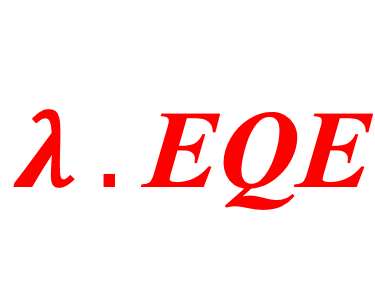
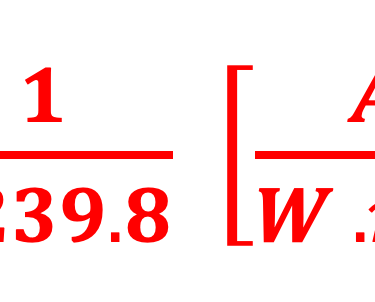

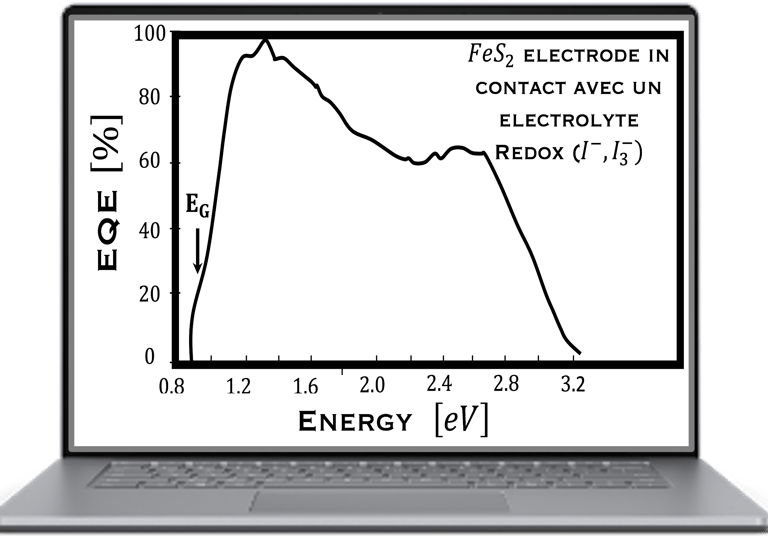
كفاءة كمية خارجية (EQE) تم قياسها على خلية كهروضوئية كيميائية من ثاني كبريتيد الحديد في محلول الأكسدة والاختزال القائم على اليود. تظهر كفاءة الكم الخارجية بداية فجوة النطاق وفقدان الإلكترونات والثقوب في عن طريق إعادة التركيب. جميع التفاصيل في رسالة التأهيل للأستاذ الدكتور أحمد الناوي*. يتم استنتاج EQE باستخدام العلاقة الرياضية
بعض الملاحظات
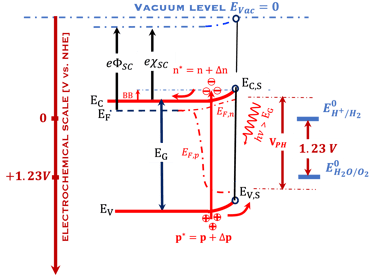
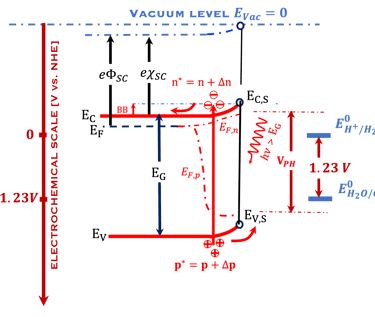
رسالة التأهيل للأستاذ الدكتور أحمد الناوي*
Habilitation thesis published in "*Ahmed Ennaoui et Al., Iron disulfide for solaZ energy conversion, Solar energy materials and solar cell, Vol. 29 (1993) 289-370"
1) المحللات الكهربائية القلوية تكنولوجيا ناضجة جدًا بالفعل والأكثر استخدامًا وتكاليفها منخفضة نسبيًا ومع ذلك، تواجه هذه التكنولوجيا مشكلة صعبة للغاية سيتطلب المزيد من البحث والتطوير ببطء والذي يعود في النهاية إلى الاستجابات البطيئة للتغيرات في الاستجابات للإمدادات في الطاقة الكهربائية وهو أمر غير متوافق مع انقطاع الطاقة الشمسية وطاقة الرياح (الرسم التخطيطي على اليسار)، مما لا يتوافق مع انقطاع (Intermittence) الطاقة الشمسية وطاقة الرياح
2) غشاء التبادل البروتوني المحلل الكهربائي للماء (WEPEM) تكنولوجيا متقدمة جدًا في مجال تحليل المياه بالكهرباء من أكبر مزايها هو القدرة على العمل عند كثافات تيار عالية والتشغيل بالضغط. يمكن أيضًا تشغيل وإيقاف المحلل الكهربائي في فترة زمنية قصيرة جدًا مقارنة بأجهزة التحليل الكهربائي القلوية. هذا يؤدي إلى خفض تكاليف التشغيل، وخاصةً عند استخدام الطاقات المتجددة ( مثل طاقة الرياح والطاقة الشمسية) والتي لديها ديناميكيات متغيرة للغاية. تعتمد خصوصية كل مُحلل كهربائي أولاً على مادة الإلكتروليت المستخدمة، والعناصر الأخرى التي سيتم شرحها هنا
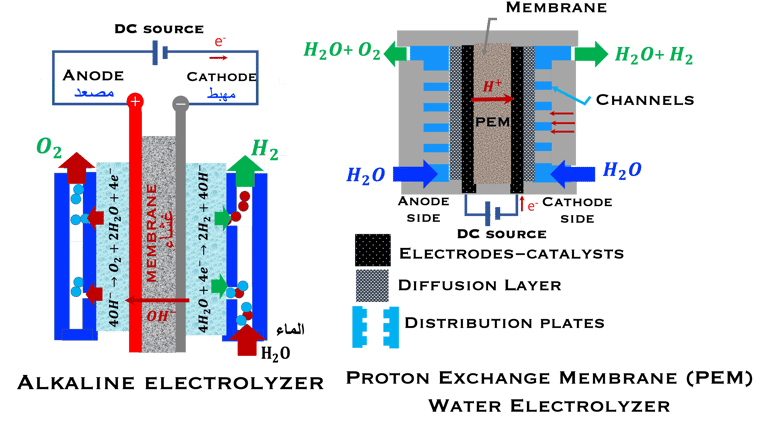
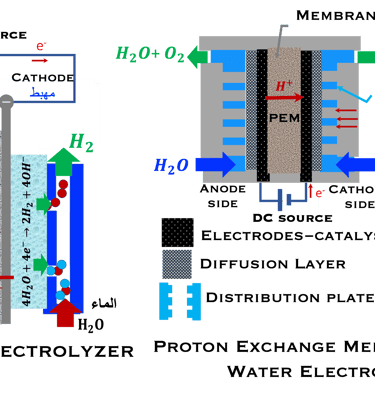
المحللات الكهربائية القلوية
الرسم التخطيطي الأيسر: يقدم توضيح للمحلل الكهربائي القلوي. وهو نوع من الأجهزة الكهروكيميائية التي تستخدم محلول قلوي سائل عادةً هيدروكسيد البوتاسيوم (30% من KOH)أو هيدروكسيد الصوديوم (NaOH) ومواد أساسها النيكل (Ni) كأقطاب كهربائية ويمكن أن يكون هذا بديلاً منخفض التكلفة بدلاً من المحفزات الكهربائية القائمة على مجموعة البلاتين المعدنية.. كما أن الخلية تحتوي على غشاء خاص يفصل الغازات المنتجة ويسمح بنقل أيونات الهيدروكسيد عبر الإلكتروليت من القطب السالب (Cathode) إلى القطب الموجب (Anode). يمكن تشغيل نظام التحليل الكهربائي بالطاقة الشمسية وطاقة الرياح، وبالتالي إنتاج الهيدروجين الأخضر
المحللات الكهربائية القائمة على غشاء تبادل البروتون
الرسم التوضيحي الأيمن: يسلط الضوء على المحلل الكهربائي للماء باستخدام غشاء التبادل البروتوني (WEPEM). هذا النوع من المحلل الكهربائي يستخدم غشاءً رقيقًا للغاية لتبادل ولنقل البروتونات مع السماح بضغوط عالية وكفاصل لعزل القطب السالب عن القطب الموجب. يُعد الغشاء "الحمضي" عنصرًا مهمًا إنه موصل بروتوني، مُغطى بطبقة رقيقة مسامية من المحفز الكهربائي على سطحي الأنود والكاثود، وهو مكون أساسي في جهاز التحليل الكهربائي، إذ يسمح بحدوث التفاعلات الكهروكيميائية النصفية في حجرات منفصلة للغازين الهيدروجين والأكسجين وتتميز هذه المواد بنقاء عالٍ، أيضًا استخدام أغشية فائقة الرقة يسمح للبروتونات بالانتقال لمسافات قصيرة، مما يقلل المقاومة الأومية (Low ohmic resistance)
سوف نسلط الضوء هنا على الأنواع الرئيسية لتقنية التحليل الكهربائي للمياه الموجودة بالفعل في مجال الصناعة:






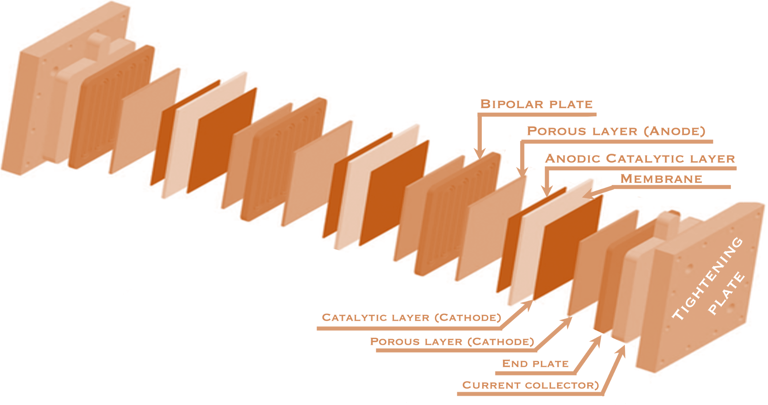
العناصر المختلفة في غشاء التبادل البروتوني (PEM) ووظائفها
نعرض أدناه محلل كهربائي (يتعلق بغشاء تبادل البروتون) ويتكون من عدة عناصر أساسية ، بما في ذلك:
لوحة الضغط، (Tightening plate) وهي صفائح طرفية تُصنع غالبًا من سبيكة الألومنيوم (Aluminium Alloy) وتستخدم لتثبيت خلية التحليل الكهربائي بأكملها
غشاء رقيق موصل للبروتونات، يفصل بين جزئي الأنود والكاثود في جهاز التحليل الكهربائي. ويسمح الغشاء بمرور أيونات الهيدروجين الموجبة (البروتونات) فقط، في حين يمنع مرور الإلكترونات السالبة.
الأنود (القطب الموجب) والكاثود (القطب السالب): الأنود هو القطب الذي يتأكسد عنده الماء لإنتاج غاز الأكسجين وأيونات الهيدروجين الموجبة (البروتونات). عادةً ما يُصنع هذا القطب الموجب من معدن مقاوم للتآكل، مثل التيتانيوم أو البلاتين. أما الكاثود فهو القطب الذي تتفاعل عنده إلكترونات وبروتونات القطب لإنتاج غاز الهيدروجين. كما يُصنع الكاثود عادةً من معدن مقاوم للتآكل، مثل البلاتين.
صفائح ثنائية القطب: عبارة عن ألواح رفيعة ومسطحة تعمل كأقطاب كهربائية في المحلل الكهربائي وتساعد أيضًا في توزيع غازات الهيدروجين والأكسجين بالتساوي. تصنع الألواح ثنائية القطب عادةً من مادة موصلة ، مثل الجرافيت أو الفولاذ (Stainless steel) المقاوم للصدأ. هناك أيضا قنوات التدفق مصممة على اللوحين ثنائيي القطب وطبقتي انتشار الغاز. كما هو موضح في الرسم التخطيطي أدناه يتم تجميع العناصر معًا في حالة مضغوطة لتجنب جميع تسرب المواد التفاعلية
كما أشرنا في بداية هذا الدليل الإلكتروني، لا تزال صناعة إنتاج الهيدروجين من الغاز الطبيعي تهيمن على السوق مع حوالي الربع يأتي من الفحم والباقي من الغاز الطبيعي مما يُسبب تلوثًا بيئيًا كبيرًا. وبلغ الطلب العالمي على الهيدروجين 97 مليون طن في عام 2023. يُستخدم الهيدروجين في قطاعي التكرير والكيماويات، وفي توليد الحرارة والطاقة. (بيانات الوكالة الدولية للطاقة المتجددة ووكالة الطاقة الذرية الأمريكية). من المهم أن نلاحظ أن إنتاج الهيدروجين المنخفض الانبعاثات بلغ أقل من مليون طن في عام 2023 ومن المتوقع أن يتزايد عدد المشاريع التي اتخذت قرار الاستثمار في إنتاج الهيدروجين من الطاقة المتجددة (الهيدروجين الأخضر والهيدروجين منخفض الانبعاثات)، حيث بلغت سعة التحليل الكهربائي المُعلنة حوالي 520 جيجاوات. كما يتزايد عدد المشاريع التي اتخذت قرار الاستثمار النهائي: فقد تضاعف الإنتاج المعلن عنه مقارنة بالعام الماضي ليصل إلى 3.4 مليون طن سنويًا، ويتوزع هذا الإنتاج بالتساوي تقريبًا بين التحليل الكهربائي (1.9 مليون طن سنويًا) والوقود الأحفوري مع التقاط الكربون واستخدامه وتخزينه (CCUS) (1.5 مليون طن سنويًا). ووفقًا للنشر الذي يظهر في سيناريو صافي الانبعاثات الصفرية بحلول عام 2050 الذي وضعته الوكالة الدولية للطاقة، تنخفض تكلفة إنتاج الهيدروجين منخفض الانبعاثات من الكهرباء المتجددة إلى 2-9 دولار أمريكي/كغ من الهيدروجين بحلول عام 2030 - أي نصف القيمة الحالية - مع تضييق فجوة التكلفة مع الإنتاج القائم على الوقود غير الأحفوري من 1.5-8 دولار أمريكي/كغ من الهيدروجين اليوم إلى 1-3 دولار أمريكي/كغ من الهيدروجين بحلول عام 2030. علينا أن نأخذ في الاعتبار أنه مع انخفاض أسعار الغاز الطبيعي في العديد من المناطق، فإن إنتاج الهيدروجين منخفض الانبعاثات من الغاز الطبيعي مع احتجاز ثاني أكسيد الكربون وتخزينه سيشهد أيضًا انخفاضًا في التكلفة.
إنخفاض تكلفة الكهرباء لا يكفي في حد ذاته لإنتاج الهيدروجين الأخضر التنافسي، وهناك حاجة أيضًا إلى خفض تكلفة مرافق التحليل الكهربائي
تأثير الهيدروجين الأخضر في تحقيق التنمية المستدامة وتعزيز الاقتصاد المغربي
يلعب الهيدروجين الأخضر دورًا محوريًا في خطط الطاقة الشمسية المغربية الرامية إلى تحقيق تحول الطاقة بنجاح وتحقيق أهداف حماية البيئة. الهدف هو استخدام الهيدروجين الأخضر في قطاعي الصناعة والنقل لتحقيق استقلالية أكبر في مجال الطاقة، وتقليل الاعتماد على الوقود الأحفوري المصدر الرئيسي لانبعاثات ثاني أكسيد الكربون، والذي يُكلف البلاد مبالغ طائلة. يتطلب هذا جذب الاستثمارات المحلية والأجنبية لبناء بنية تحتية قوية ومحطات لتحليل الماء ومرافق تخزين الهيدروجين. يعد البحث والتطوير أمرًا بالغ الأهمية في نجاح طرح تقنيات التحليل الكهربائي وكقوة دافعة نحو التصنيع بخبرة مغربية. هناك الكثير من العمل في المستقبل لإيجاد مواد فعالة للأقطاب الكهربائية والأغشية والحفازات، تصميم أجهزة التحليل الكهربائي المعيارية التي يمكنها العمل تحت كثافة تيار أعلى لفترة طويلة لضمان أداء جهاز التحليل الكهربائي على مدى عمر طويل بما يكفي تقليل وقت الاسترداد وخفض التكلفة
معلومات عامّة
يمكن أن تؤدي زيادة حجم المحلل الكهربائي من 1 ميجاوات (الحجم المعتاد اليوم) إلى 20 ميجاوات إلى خفض التكاليف بأكثر من الثلث
تمثل ندرة المواد عائقًا أمام تكلفة المحلل الكهربائي وتوسيع النطاق من النموذج الأولي إلى التصنيع. على سبيل المثال، يمكن أن يحد الإنتاج الحالي للإيريديوم والبلاتين كمحفزات للمحللات الكهربائية التي تستخدم غشاء التبادل البروتوني (PEM) من التوسع فوق 7.5 جيجا وات

أدعو الزوار لمشاهدة هذا الفيديو قبل الانتقال إلى الدورات القادمة. تم تقديم هذا المؤتمر عبر الإنترنت ضمن مؤتمرات أخرى من أنشطة جامعة التعليم الافتراضي ألقاها توماس هانابيل وهو أستاذ في جامعة إلميناو التقنية، معهد الفيزياء، ألمانيا؛ وسلّط الضوء على الخلفيات الأساسية المتعلقة بالتمثيل الضوئي الاصطناعي. تقسيم الماء إلى الهيدروجين والأكسجين من خلال استخدامات العملية الكهروكيميائية الضوئية، هو في الواقع نوع من تقليد الطبيعة (التمثيل الضوئي الاصطناعي)*. كما هو موضح في الوثائق أعلاه تستخدم أقطابًا شبه موصلة في خلية كهروضوئية لتحويل طاقة الفوتونات إلى طاقة كيميائية. إنه تحويل مباشر دون استخدام الألواح الشمسية ولا تزال هذه الطريقة في مرحلة البحث والتطوير، على الرغم من أن إثباتات المفهوم ذات الكفاءة العالية في تحويل الطاقة إلى طاقة (الهيدروجين) واعدة جدًا (ننصح الزوار بمشاهدة فيديو وندوات توماس هانابيل عبر الإنترنت المتوفر هنا )
في يوليو 2018، تم نشر رقم قياسي بنسبة 19.3% (انظر الندوة التي عقدها توماس هانابل، أحد مؤلفي المقال) مع فريق كامل مكون من معهد كاليفورنيا للتكنولوجيا وجامعة كامبريدج وجامعة إلميناو التقنية (توماس هانابل) ومعهد فراونهوفر لأنظمة الطاقة الشمسية ISE، وكذلك معهد الوقود الشمسي في مركز هيلمهولتز برلين الذي شارك في التجربة
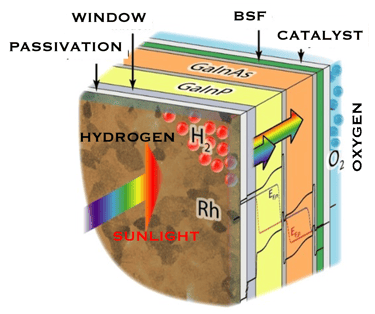
Innovation in R&D: Collecting the maximum of solar spectrum consists of using a multi-junction electrode
Integration of light absorption and electrolysis into a single device may significantly reduce the total system costs
Selected catalysts for the hydrogen (HER) and oxygen evolution reactions (OER)
Photoelectrode for water splitting using multifunction with GaInP, and GaInAs and electrocatalysts
Solar RRL, Volume: 8, Issue: 11, First published: 18 March 2024, DOI: (10.1002/solr.202301047)
https://onlinelibrary.wiley.com/doi/full/10.1002/solr.202301047
Solar-To-Hydrogen conversion efficiency of 19% are published recently by Thomas Hanappel et al.
*التمثيل الضوئي الاصطناعي هو عملية امتصاص الضوء وفصل الشحنة باستخدام تكنولوجيا تعتمد على وحدات تحفيزية للأكسدة والاختزال بالماء بما في ذلك اختزال ثاني أكسيد الكربون.
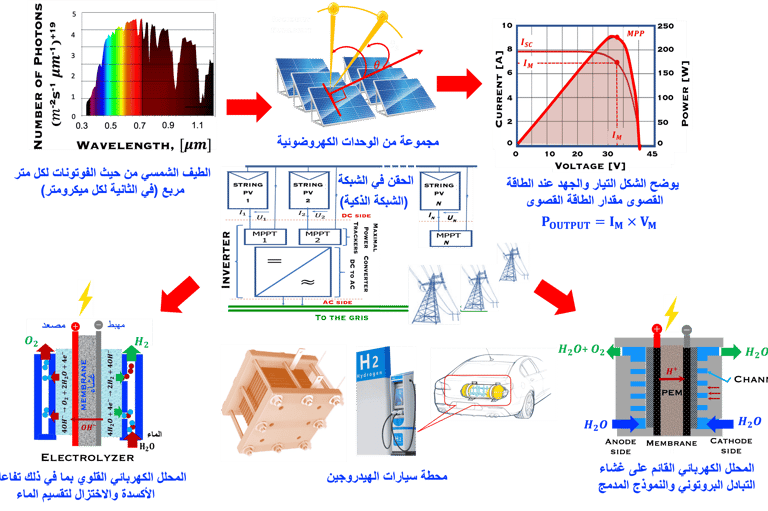
محلل كهربائي قلوي، يشمل المعدات التي تُشغّل الجهاز الكهروكيميائي وتُزوّده بالكهرباء من الشبكة الذكية. تحدث التفاعلات الكهروكيميائية، وتُسرّع المحفزات عمليات تفكيك الماء إلى هيدروجين وأكسجين. يُنتج النظام الكهروضوئي الكهرباء عن طريق امتصاص ضوء الشمس من الطيف الشمسي وتُضخ الكهرباء إلى الشبكة بعد تحويل التيار المستمر (DC) إلى تيار متردد (AC) وتسمح الشبكة الذكية بتحويل فائض الكهرباء إلى تيار مستمر (DC)، لتشغيل المحللات الكهربائية، مثل المحللات الكهربائية القلوية وأجهزة غشاء تبادل البروتونات لإنتاج الهيدروجين والأكسجين
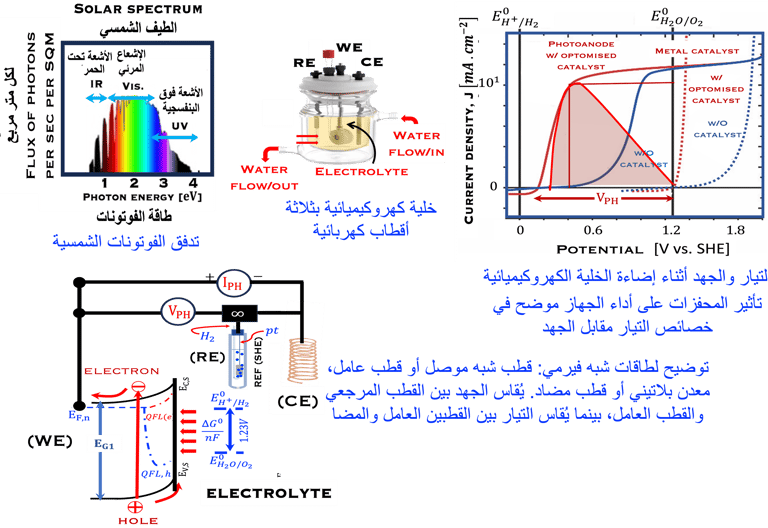
خلية كيميائية كهروضوئية: نظام مكوّن من قطب كهربائي عامل (شبه موصل)، وقطب كهربائي مضاد (قطب معدني)، وقطب كهربائي مرجعي (SHE) . يتم اختيار أشباه الموصلات لامتصاص تدفُّق الفوتونات الشمسية الساقطة، يؤدي إلى إنشاء ثقوب على نطاق التكافؤ وإلكترونات على نطاق التوصيل، هذا يؤدي إلى جهد وتيار. يتيح الإختيار الدقيق لأشباه الموصلات من حيث الخصائص الإلكترونية ظهور جهد كهربائي كافٍ لتحليل الماء، استخدام المحفزات على سطح الأقطاب الكهربائية أمر ضروري لتسريع الاختزال والأكسدة الكهروكيميائية وأداء أفضل من حيث كفاءة الهيدروجين
نقارن نقارن بين نظامين مختلفين: التكنولوجيا الناضجة (PV-Electrolyser) مع التكنولوجيا الناشئة القائمة على محاكاة الطبيعة (الخلية الشمسية الكهروكيميائية الضوئية)
فهم كفاءة الطاقة في تحويل ضوء الشمس إلى منتجات كيميائية: على سبيل المثال، كفاءة تحويل الطاقة الشمسية إلى هيدروجين أو الاختزال الكهروكيميائي لثاني أكسيد الكربون (تعقيدات ”الطاقة إلى X“)
القطب السالب شبه موصل (نوع P) مصدر نصف التفاعل الكهروكيميائي الآخر لاختزال بروتونات الهيدروجين

القطب الموجب شبه موصل (النوع N) مصدر نصف التفاعل الكهروكيميائي لأكسدة الماء

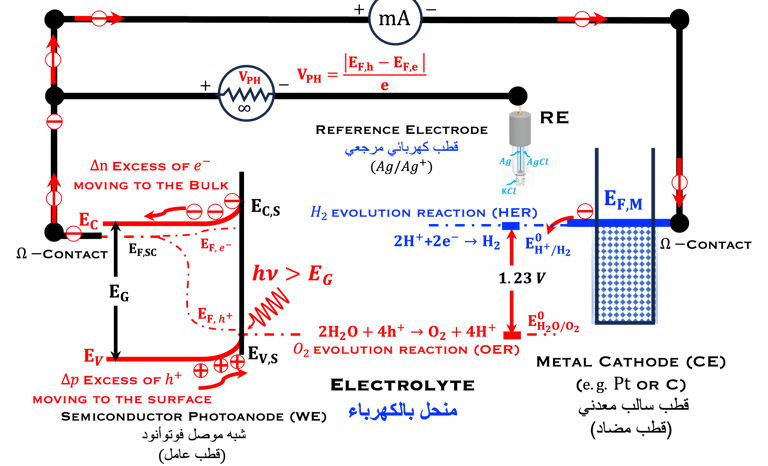
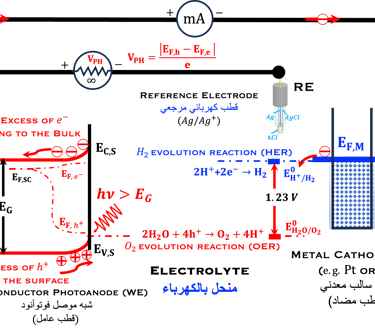
يشير الرسم التوضيحي أعلاه إلى الظروف من وجهة نظر مقياس الطاقة مواتية لأكسدة الماء إلى جزيئات الأكسجين واختزال بروتون الهيدروجين إلى جزيئات الهيدروجين. النطاق لأشباه الموصلات كبيرة بما يكفي مقارنة بجهد الأكسدة والاختزال
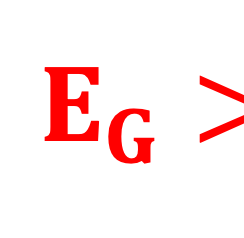
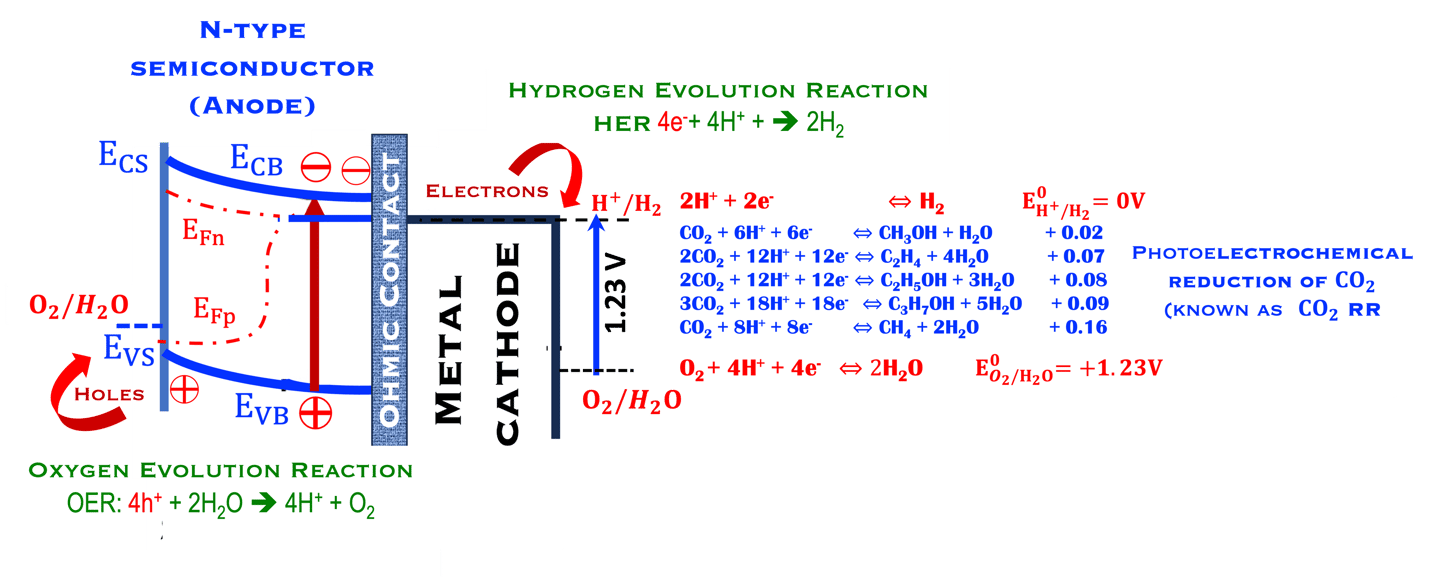
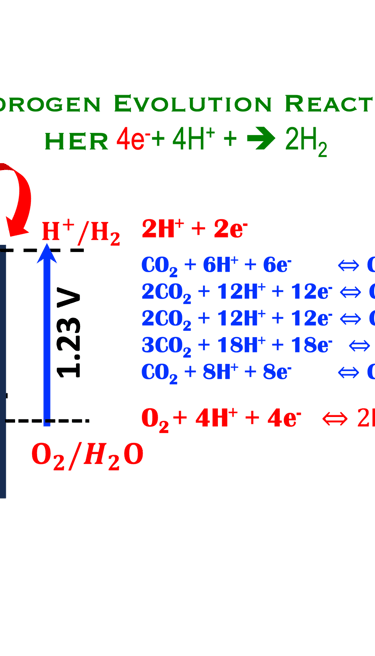
يوضح الرسم التوضيحي أدناه تعقيدات الطاقة إلى X، هنا اخترنا أكسدة الماء، واختزال بروتون الهيدروجين، والاختزال الكهروكيميائي لثاني أكسيد الكربون. هناك أبحاث واسعة النطاق تركز على الفهم الأساسي لآليات التحفيز والتفاعل. يخضع الاختزال الكهروكيميائي لثاني أكسيد الكربون لعمليات معقدة إلى حد ما، ويمكن أن يتم من خلال مسار اختزال ثنائي أو رباعي أو ستة أو ثمانية أو اثني عشر أو حتى ثمانية عشر إلكترونًا لإنتاج منتجات غازية مختلفة مثل الميثان والإيثيلين والمنتجات السائلة مثل حمض الفورميك والميثانول والإيثانول والبروبانول
من خلال إلقاء نظرة بسيطة على معادلات الاختزال الكهروكيميائية وجهد الاختزال الديناميكي الحراري في الرسم التوضيحي (على اليمين)، نلاحظ عندما يتم إجراء اختزال ثاني أكسيد الكربون في بيئة مائية، نرى بوضوح أن التعقيد يأتي أولاً من تفاعل تطور الهيدروجين المتنافس مع تفاعل اختزال ثاني أكسيد الكربون هو أيضا يمكن اختزاله كهروكيميائيًا إلى عدة منتجات عند جهد ترموديناميكي متقاربين جدًا مع بعضهم البعض، السؤال ذو طابع اقتصادي إلى حد ما: ما هو منتج اختزال ثاني أكسيد الكربون الذي ينبغي استهدافه للتسويق؟ أشار إلى هذا السؤال ماثيو جوني وآخرون من جامعة ديلاوير، الولايات المتحدة الأمريكية، وتم نشر تحليل تقني اقتصادي عام لأنظمة التحليل الكهربائي لثاني أكسيد الكربون. لمزيد من التفاصيل،
يرجى زيارة الرابط (source: https://www.osti.gov/pages/servlets/purl/1712664).
من التحديات الأخرى الاستقرار الديناميكي الحراري لجزيء ثاني أكسيد الكربون المؤكسد بالكامل، لذا تُعد المحفزات ضرورية لتسهيل التحول الكيميائي وتقليل استهلاك الطاقة اللازم لاختزال ثاني أكسيد الكربون.
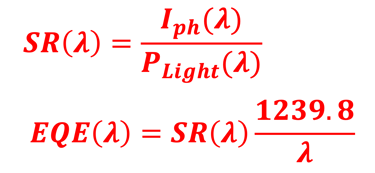
بشكل عام، كفاءة فاراداي (ηF: Faraday EFFICIENCY) هي قياس لانتقائية منتج كهروكيميائي مُحدد أثناء التحليل الكهربائي. يمكن النظر إليها على أنها كفاءة التيار الكهروكيميائي لمنتج معين. يمكن التعبير عنها كالشحنة الخاصة بمنتج معين (n.N.F) على الشحنة الكهربائية الإجمالية للعملية الكهروكيميائية. على سبيل المثال، الكفاءة الفرادية لناتج معين هي انتقائية اختزال بروتونات الهيدروجين أو اختزال ثاني أكسيد الكربون إلى هذا الناتج.
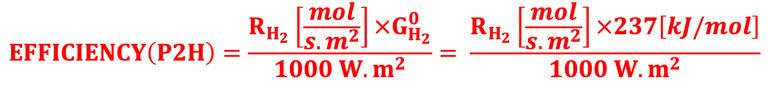
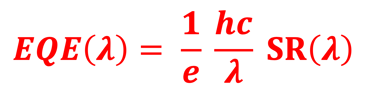
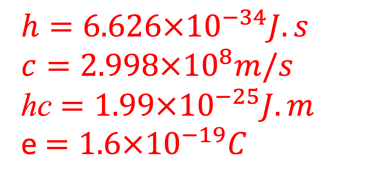
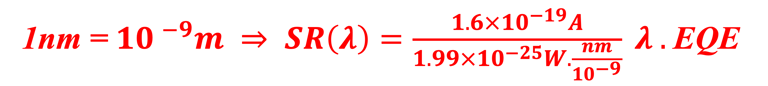
ملاحظة 1 : الطريقة الأكثر مباشرة لتحديد كفاءة الطاقة الشمسية إلى الهيدروجين هي قياس كمية الهيدروجين المتطور باستخدام تقنية الغاز الكروماتوغرافيا
ملاحظة 2 : يمكن تعريف كفاءة تحويل الطاقة الشمسية إلى هيدروجين (STH) للخلايا الشمسية الكهروضوئية الكيميائيةبناءً على معايير أخرى، مثل كفاءة فراداي:
علاقة رياضية مهمة، تربط كفاءة الكم (EQE) بالاستجابة الطيفية (SR)
عادةً، نستخدم المقاييس الذرية:. الأطوال الموجية معبر عنها بالنانومتر، وطاقة الفوتون الساقط بالإلكترون فولت
كفاءة تحويل الطاقة الشمسية إلى هيدروجين: معدل إنتاج الهيدروجين مقسومًا على طاقة جيبس الحرة لتكوين الهيدروجين
( POWER TO HYDROGEN EFFICIENCY )
الكفاءة الكمية: عدد الإلكترونات التي تُنتج تيارًا كهروكيميائيًّا عند الإضاءة مقسومًا على عدد الفوتونات الساقطة على القطب شبه الموصِّل
( QUANTUM EFFICIENCY )


(1) في ظل الظروف المثالية، مع أقصى كفاءة فاراداي، تكون كمية الهيدروجين المتولدة ضعف كمية الأكسجين من حيث عدد المولات كماكما هو موضح في التفاعل الشامل لانقسام الماء، وويجب أن يكون متناسبا مع الشحنة الكهربائية التي تمر عبر المحلول
(2) في معادلة كفاءة فاراداي (η) عدد مولات الإلكترونات المطلوبة (يشار إليه n) لتكوين مول واحد من المنتج (بالنسبة للهيدروجين, اختزال بروتونين إلى مول واحد من الهيدروجين وعدد مولات المنتج (يشار إليه N) المتكون أثناء اختزال البروتونات وثابت فاراداي (F=96500C)
(3) كيفية تحديد كفاءة فاراداي تجريبياً: للحصول على قيمة دقيقة لكفاءة فاراداي (η)، لا بد من التحديد الكمي الدقيق لمنتجات التفاعلات الكهروكيميائية. هناك عدة تقنيات للتحليل الكيميائي للمنتجات، الكروماتوغرافيا الغازية هي واحدة من أكثر تقنيات التحليل شمولا كتقنية تحليلية لتحديد كمية المنتجات الغازية مثل الهيدروجين. تقدم هذه التقنية حساسية عالية وكفاءة فصل ممتازة وتنوعًا وسرعة وإمكانية التشغيل الآلي، مما يجعلها الخيار المفضل للبحث والتطوير. المصدر:
ACS Energy Lett. 2024, 9, 323−328
أكسدة مول من الماء
اختزال بروتونات الهيدروجين
التفاعل الشامل لانقسام الماء




عدد مولات الإلكترونات اللازمة للحصول على جزيء واحد من المنتج (𝑛𝑒)
جزء في المليون من المنتجات الغازية المتكونة (𝑥)
درجة الحرارة (T) كلفن 298.15
ثابت فاراداي (F = 96500 C) ؛ ثابت الغاز (R) = 8.314 جول لكل كلفن لكل مول
الضغط الجوي القياسي (P): 101325 باسكال
(𝐼) كثافة التيار وقت أخذ العينات
الروتين التجريبي الذي يجب اتباعه
نأخذ في الاعتبار ما يلي: كمية غاز معين Np مول
حجم حلقة العينة المستخدمة في كروماتوغرافيا الغاز V
معادلة قانون الغاز المثالي: كمية الغاز (n) المراد قياسها (n=PV/RT). في ظروف الضغط ودرجة الحرارة P و T
في هذا التحليل المنتج المكتشف هو: (𝑥) جزء في المليون ،
كميات مولات المنتج الغازي ستكون: (Np = 𝑥 . n / 1000000)
عدد مولات الإلكترونات المطلوبة للحصول على كمية من البروتونات المختزلة إلى ناتج هيدروجين هو: 𝑁𝑝 × عدد مولات الإلكترونات اللازمة للحصول على مول واحد من الناتج (e)n
العدد الإجمالي لـ مولات الإلكترونات المنقولة خلال زمن أخذ العينة 𝑡 هو: I x t/F = e(t)
(𝑡 = V/flow rate) الوقت المطلوب لملء حجم حلقة العينة
هو التيار أثناء وقت أخذ العينة (𝐼)


المقياس الذي يعكس كفاءة الخلية الكهروكيميائية الضوئية (PEC) في تحويل الفوتونات الممتصة إلى إلى تيار كهربائي يُعرف بالكفاءة الكمية (𝝀)EQE. بعبارة أخرى القدرة على امتصاص أقصى قدر من الطيف الشمسي وتحويله إلى تيار كهروكيميائي. يمكن أن يستهلك التيار الكهربائي في التفاعلات الكهروكيميائية مثل اختزال بروتونات الهيدروجين وإنتاج الهيدروجين الأخضر، وذلك اعتمادًا على أداء المحفزات. مقياس ذلك هو كفاءة التحويل (الطاقة إلى H). تعتمد كمية الهيدروجين المنتجة أيضًا على أشعة الشمس الممتصة، ولكن أيضًا على معايير أخرى مثل كفاءة فاراداي. سيتم تسليط الضوء على الفهم العميق بما في ذلك قياسات جميع هذه العناصر
يجب عدم الخلط بين الكفاءة الكمية (𝝀) EQE وكفاءة تحويل الطاقة الشمسية إلى هيدروجين
( POWER TO HYDROGEN EFFICIENCY )
للتمييز بين الكفاءة الكمية (𝝀) EQE ووكفاءة تحويل الطاقة الشمسية إلى هيدروجين ( POWER TO HYDROGEN EFFICIENCY ) ، من المهم ملاحظة أن يجب أن نعود إلى ما معنى الطاقة الحرة لانقسام. التغيُّر في طاقة جيبس الحرة هو القوة الدافعة لتقسيم الماء بمقدار 237 كيلوجول/مول مما ينتج عنه جهد الأكسدة والاختزال من قيمة 1.23 فولت. نفترض أن ضوء الشمس الساقط AM1.5G (1000 واط/متر مربع) وبدون جهد كهربائي خارجي آخر
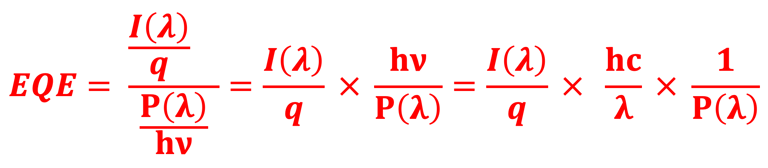
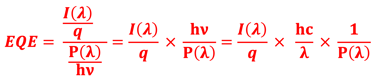
كفاءة فاراداي، لناتج معين، هي انتقائية اختزال بروتونات الهيدروجين أو اختزال ثاني أكسيد الكربون إلى ذلك الناتج
معلومات عامة مفيدة
بلغت سعة المحللات الكهربائية المركبة عالميًا 1.4 جيجاوات (GW) في نهاية عام 2023، ومن المتوقع أن تصل سعة المحللات الكهربائية المركبة إلى 230-520 جيجاوات بحلول عام 2030. تتطلب تكنولوجيا المحلل الكهربائي الكثير من الإنجازات العلمية والتطورات التكنولوجية خاصةً تطوير محفّزات جديدة مواد منخفضة التكلفة مثل (Fe، Co، Ni، Ni، Cu، Zn، Ti) وخفض تكاليف التصنيع، والتوجه نحو اقتصاد الحجم (Economy of scale) التي تؤدي إلى خفض تكاليف المحلل الكهربائي . من المتوقع أن ينمو سوق المحلل الكهربائي ليصل إلى قيمة تقديرية تبلغ 306.91 مليون دولار أمريكي بحلول عام 2032، مدفوعًا بالطلب المتزايد على الهيدروجين من أجل مستقبل مستدام. يلتزم المغرب التزامًا كبيرًا بتطوير الهيدروجين الأخضر باستخدام المحلل الكهربائي، وإزالة الكربون من الصناعة في البلاد ووفقًا لمجلة (PV-Magazine) وافقت الحكومة المغربية على ستة مشاريع من قبل مجموعة من الشركات الأجنبية، في حين اجتذب المزاد الثاني لبنك الهيدروجين الأوروبي لإنتاج الهيدروجين المتجدد 61 عرضًا من مشاريع في 11 دولة. هذه السياسة من شأنها أن تساعد المغرب على ”لعب دور رئيسي في مجال التحول الطاقي على الصعيد العالمي“
وجد باحثون هولنديون بتحليل أكثر تقنيتين واعدتين لإنتاج الهيدروجين الأخضر بمساعدة الطاقة الشمسية، استنادًا إلى التكلفة المستوية للهيدروجين، أن إنتاج الهيدروجين الذي يعمل بالطاقة الكهروضوئية يوفر أقل التكاليف، حيث تبلغ التكلفة 6.22 دولار/كجم، مع نسبة كفاءة من الطاقة الشمسية إلى الهيدروجين تبلغ 10.9%. دراسات اقتصادية منشورة في المجلة الدولية لطاقة الهيدروجين: Alexa Grimm et al. in International journal of hydrogen energy 45 (2020) 22545-22555
https://www.pv-magazine.com/2020/08/12/photo-electrochemical-cells-vs-pv-electrolysis/
نُشرت هذه المعلومات في مجلة (PV Magazine)، حيث قارن فريق البحث من جامعة أوتريخت في هولندا بين تقنيتين واعدتين لإنتاج الهيدروجين بمساعدة الطاقة الشمسية: الأنظمة الكهروكيميائية الضوئية (PEC) التي تحوّل الإشعاع الشمسي مباشرة إلى هيدروجين، والمحللات الكهربائية الكهروضوئية التي تعمل بالطاقة الكهروضوئية خارج الشبكة. لوصف أداء التقنيات، تم استخدام كفاءة الطاقة الشمسية إلى الهيدروجين، كما هو موضح أعلاه في تعريف كفاءة الطاقة الشمسية إلى الهيدروجين. وتستند النتائج إلى التكلفة المحسوبة بالقيمة المستوية للهيدروجين (LCOH) لكلتا التقنيتين من خلال النظر في التصاميم القياسية للطاقة الكهروضوئية - الكهربائية والتصاميم المتوقعة للتطبيقات المستقبلية واسعة النطاق.
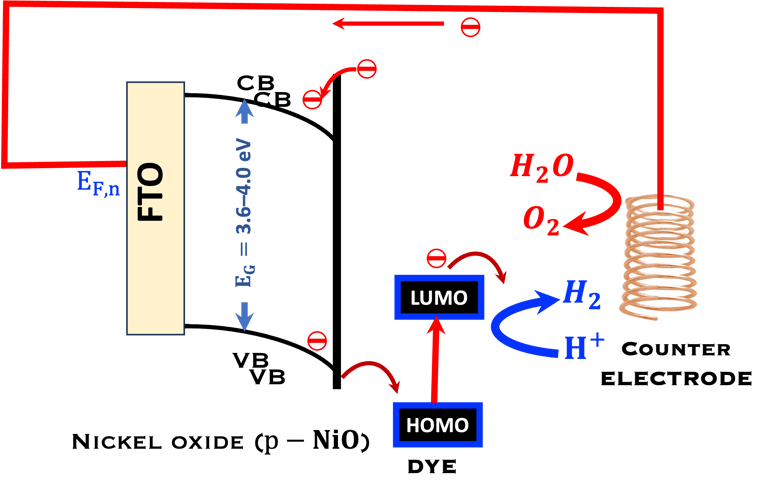
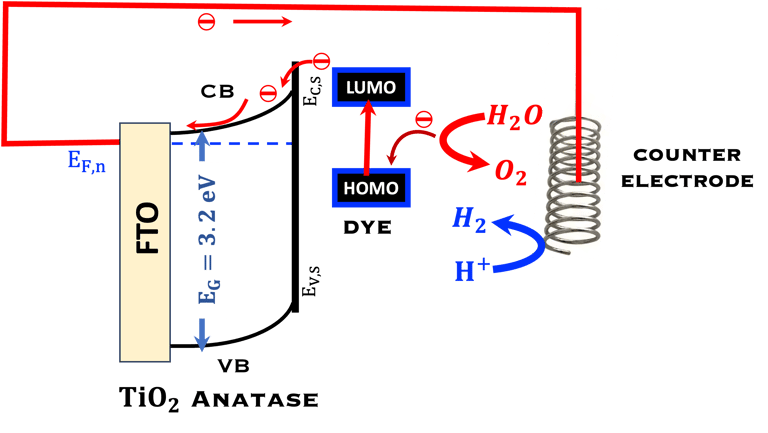
نسلط الضوء هنا على مثال للخلية الكهروكيميائية الضوئية (PEC) لشرح التشابه مع التمثيل الضوئي الاصطناعي
الرسوم التوضيحية أدناه تمثل الرسوم التوضيحية أدناه شكلين توضيحيين مشابهين للبناء الضوئي الأمر كله يتعلق بـالخلايا الشمسية الحساسة للصباغة والتي يشار إليها غالبًا باسم "خلية غريتزل" اسم مخترع هذا النوع من الخلايا الشمسية سنة 1991 (Michael Grätzel). يتكون هذا النوع من الخلايا الشمسية من أشباه الموصلات ذات فجوة (Band gap) عريضة مثل ثاني أكسيد التيتانيوم (الأناتاز) وصبغة ممتزّة على سطح ثاني أكسيد التيتانيوم. تتميز تتميز الصبغة العضوية بأعلى مدار جزيئي مشغول (HOMO) إلى أدنى مدار جزيئي غير مشغول (LUMO) كما هو موضح في الرسم التخطيطي. تحت الإضاءة، تتلقى الإلكترونات طاقة من الفوتونات وتمر من حالة الطاقة المنخفضة (HOMO) إلى حالة الطاقة العالية (LUMO) يليها الحقن في نطاق التوصيل لثاني أكسيد التيتانيوم، والإنتقال إلى القطب المضاد عبر الدائرة الكهربائية الخارجية. إن وجود المحفزات المختارة بشكل صحيح يمكّن من تقسيم الماء إلى أكسجين وهيدروجين، وكذلك تفاعلات كهروكيميائية الأخرى مثل الاختزال الكهروكيميائي لثاني أكسيد الكربون. المشكلة مع هذا النوع من الأجهزة هي عدم الاستقرار على المدى الطويل
سيصدر قريباً
الرابطة الثلاثية الماء والطاقة والغذاء
في خطابه لافتتاح الدورة الأولى من السنة التشريعية الثانية من الولاية التشريعية الحادية عشرة، أكد جلالة الملك كان الله في عونه وتوفيقه أن “الحالة الراهنة للموارد المائية، تسائلنا جميعا، حكومة ومؤسسات ومواطنين وتقتضي منا التحلي بالصراحة والمسؤولية في التعامل معها، ومعالجة نقط الضعف، التي تعاني منها”


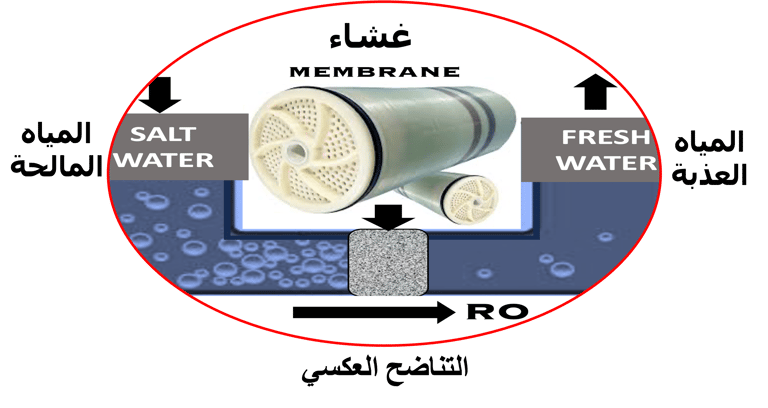
تحويل المياه المالحة وإزالة ملوحتها ومعالجتها تحويها إلى مياه عذبة
تُستخدم العديد من التقنيات لتحويل المياه المالحة إلى مياه عذبة
حلول مستدامة لمحطات تحلية المياه باستخدام تقنية التناضح العكسي
تمثل المياه المستخرجة من المحيطات والبحار الساحلية ومستودعات المياه الجوفية المالحة والبحيرات المالحة المغلقة أكثر من 97% من مياه الأرض (ويكيبيديا)مالحة
عملية التحلية الأكثر استخداماً هي التقطير، وتعتمد على الطاقة الحرارية. في المرحلة الأولى، يتم غلي الماء في درجة حرارة عالية جدًا، مما يؤدي إلى تبخره. ثم تليها مرحلة أخرى تتضمن تبريد البخار وتكثيفه لإنتاج ماء نقي. تكمن الصعوبة الرئيسية في استخدام هذه الطريقة في أنها تتطلب كمية كبيرة من الطاقة الحرارية

أحد الابتكارات التي لا تزال تحقق تقدماً هو التناضح العكسي، وهي عملية تزيل الملوثات الغريبة والمواد الصلبة والجسيمات الكبيرة والمعادن من المياه عن طريق دفعها، تحت الضغط، من خلال أغشية مصنوعة من مواد وظيفية. وتحت ضغط عملية التناضح العكسي، تتدفق المياه النظيفة فقط إلى الخارج، تاركة المياه القذرة وراءها. وبهذه الطريقة، يمكن استعادة المياه ومعالجتها، إذا لزم الأمر، للري والاستخدامات الهامة الأخرى
أتاحت الأبحاث الأساسية والبحث والتطوير في مجال المواد الوظيفية والمواد النانوية إمكانية التحكم في المادة على مقياس يتراوح بين 1 إلى 100 نانومتر (النانومتر هو جزء من مليون من المليمتر). وقد أدى ذلك إلى تطوير أغشية قادرة على فرز الملوثات الصناعية والجسيمات السامة الأخرى، مثل المعادن الثقيلة والبكتيريا والفيروسات المختلطة بالماء.
البحث والتطوير على الأغشية المركبة المصنوعة من مواد نانوية مسامية في التطبيقات التي تقلل بشكل كبير من استهلاك الطاقة وخطر الانسداد مقارنة بالأغشية التقليدية لنفس الغرض. على سبيل المثال، تعد أغشية الأنابيب النانوية الكربونية واعدة جدًا لتقليل استهلاك الطاقة لفصل الغازات والسوائل والملوثات.
الخلاصة - من المهم أن نلاحظ أن عمليات التناضح العكسي، التي تستخدم الطاقة الكهربائية فقط (خاصة الطاقة المتجددة)، أصبحت الخيار المفضل لمحطات تحلية مياه البحر، نظرًا لانخفاض تكاليفها الاستثمارية وتكاليف الطاقة مقارنةً بتكاليف محطات التقطير التي تستهلك الكثير من الطاقة الحرارية.



